- Thermal Properties of Diglycidyl Ether of Terephthalylidene-bis-(4-amino-3-methylphenol)
Ha-Neul Hyun*, Ji-Woo Choi*, Seung-Hyun Cho*†
Department of Organic Materials and Fiber Engineering, Soong-sil University
- Diglycidyl ether of terephthalylidene-bis-(4-amino-3-methylphenol)의 열적 성질에 대한 연구
현하늘*· 최지우* · 조승현*†
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
This study uses Diglycidyl ether of terephthalylidene-bis-(4-amino-3-methylphenol) (DGETAM), an amine hardener 4,4’-diaminodiphenylethane (DDE) and cationic catalyst N-benzylpyrazinium hexafluoroantimonate (BPH) to make epoxy film. For analysis, 1H_NMR and FT-IR were used to verify proper synthesis, and the liquid crystallinity of DGETAM was checked using Differntial Scanning Calorimetry and Polarized Optical Microscopy. Thermal conductivity of the sample was measured using Laser Flash Apparatus. Thermal stability as well as thermal conductivity is important when used as a packaging material. Activated energy is the energy needed to generate a response, which can be used to estimate the energy required to maintain physical properties. It was obtained using the Arrhenius equation based on the data measured by isothermal decomposition using Thermogravimetric Analysis. Measurement of the thermal conductivity of epoxy films showed higher thermal conductivity when DDE was used, and it was found that thermal conductivity had an effect on thermal stability, given that it represented an activation energy similar to a film with BPH upon 5% decomposition
본 연구에서 액정성 에폭시인 Diglycidyl ether of terephthalylidene-bis-(4-amino-3-methylphenol) (DGETAM)을 사용해 경화제로는 아민계 경화제인 4,4’-diaminodiphenylethane (DDE)와 양이온 개시제인 N-benzylpyrazinium hexafluoroantimonate (BPH)를 사용하여 필름의 형태로 샘플을 제작하였다. 합성의 확인을 위하여 1H-NMR과 FT-IR을 사용하였고, DSC와 POM을 이용하여 DGETAM의 액정성을 확인하고, LFA를 사용하여 샘플의 열전도도를 측정하였다. 활성화 에너지는 TGA를 사용하여 등온 열분해를 진행해 측정한 데이터를 토대로 Arrhenius 식을 사용하여 구하였다. 에폭시 필름의 열전도도를 측정한 결과 DDE를 사용하였을 때, 더 높은 열전도도를 나타내었고, 5% 분해시 BPH를 사용한 필름과 유사한 활성화 에너지를 나타내는 것으로 보아, 열전도도가 열적 안정성에 영향을 미치는 것을 확인할 수 있었다
Keywords: 열경화성 액정 에폭시(Liquid crystalline thermosetting epoxy), 열분해 활성화 에너지(Activation energy for thermal decomposition), 열전도도(Thermal conductivity)
현대 사회에서 전기전자 부품들은 점점 소형화 되고 집적화에 따라 더 높은 성능을 발휘할 수 있게 되었다[1-4]. 하지만 소형화 및 집적화에 따른 성능의 증가와 동시에 부품의 발열량 또한 증가하게 되었다[5-7]. 발열을 원활하게 제어하기 위해서는 발열체인 소자와 히트 싱크를 연결하는 패키징 소재의 열전도도와 열적 안정성이 우수해야 한다. 에폭시는 가격이 저렴하고 기계적, 화학적 물성이 우수하며, 구조 안정성과 절연성이 높아 패키징 소재로 많이 사용되고 있으나[8-10] 점도가 높아 공정 중에 기포 제가가 어렵고, 열전도도가 0.2 W/m*k로 낮은 문제가 있어 현재는 열적 물성이 높은 금속이나 탄소, 세라믹 소재 등을 충전제로 사용해 복합재로 만들어 사용되고 있다[11-13]. 그러나 충전제의 함량이 높은 복합재는 성형성과 물성이 떨어진다는 단점이 존재하며, 복합재의 열적 물성에는 충전제보다 매트릭스의 물성이 더 많은 영향을 미치기 때문에 높은 열적 물성을 갖는 소재의 개발이 요구되고 있다[14-17]. 이러한 문제점을 보완하기 위해 에폭시에 액정성을 부여한 액정성 에폭시(Liquid Crystalline Epoxy)가 연구되고 있는데, 액정성 에폭시는 기존의 에폭시 대비 전반적으로 물성이 우수하고 융점이 낮으며, 전자기장을 사용해 배향을 조절할 수 있다는 장점이 있다[20-22]. 액정을 이루는 메조젠은 충분히 경질이고 직선적인 분자들로 구성이 되며 고분자의 주쇄나 측쇄에 위치할 수 있고 일반적으로 벤젠링을 포함해 구성이 이뤄진다[23-25].
이러한 액정성 에폭시는 상용 에폭시 대비 열전도도가 우수하다는 점이 보고되어 있다[26,27]. 하지만 아민계 경화제를 사용해 경화를 진행하는 경우 결정구조에 왜곡을 발생하는 문제점이 있어 이를 보완하기 위해 양이온 개시제를 사용하여 경화를 진행할 경우 액정 구조의 왜곡을 감소시켜 열적 물성을 향상시킬 뿐만 아니라, 단시간에 반응이 진행되어 공정 시간이 단축된다는 장점이 존재한다[28,29]. 이전 연구에서 열에 의해 액정을 형성하는 열방성 액정에폭시로 Diglycidyl ether of 4,4’-Bisphenol(DGEBP)를 사용하여 고찰한데 이어 본 연구에서는 열방성 액정 에폭시인 Diglycidyl ether of terephthalylidene-bis-(4-amino-3-methylphenol) (DGETAM)과 양이온 개시제인 N-Benzylpyrazinium Hexafluoroantimonate(BPH)를 합성하고 아민계 경화제인 4,4’-diaminodiphenylethane(DDE)를 이용하여 에폭시 필름을 제조하여 고찰하였다. 경화 구조에 따른 열전도도의 변화를 확인하기 위하여, LFA-467을 사용하여 열확산 계수와 열전도도를 측정하였다. 또한 제작된 필름의 열적 안정성을 확인하기 위해 TGA를 사용하여, 열분해 활성화 에너지를 계산하였다[30,31].
2.1 시료 및 시약
4-amino-3-methylphenol, terephthalaldehyde, zinc chloride, tetra-n-butylammonium chloride, 4-amino-m-cresol은 TCI (Tokyo Chemical Industry)사에서, 4,4’-diaminodiphenylethane, pyrazine, benzyl bromide(98%), NaSbF6는 Sigma-Aldrich사에서, epichlorohydrin(99%), sodium hydroxide(98%), Acetone (98%)은 삼전화학에서 구입하였다. 모든 시약은 별도의 정제없이 사용하였다.
2.2 DGETAM의 합성
Terephthalaldehyde 12 g, 4-amino-3-methylphenol 23.33 g, zinc chloride 0.33 g, ethyl alcohol 150 ml을 3구 플라스크에 넣고, 80oC를 유지하면서 질소 기류 하에 마그네틱 바를 사용해 300 rpm으로 4시간 교반한다. 교반 후, 상온에서 12시간가량 식힌 다음 노란색의 고체(TAM)를 methyl alcohol과 distilled water을 사용하여 수세한다. 수세한 물질을 60oC 진공오븐에서 6시간 이상 건조한다. 전구체 TAM 12 g, tetra-n-butylammonium chloride 0.26 g epichlorohydrin 56 ml, dimethyl sulfoxide 100 ml을 3구 플라스크에 넣고 마그네틱 바를 사용하여 교반한다. 온도는 80oC를 유지하며 질소 기류 하에 환류를 시켜 가열한다. 충분한 교반 후 투명해지면 1.5 mol% NaOH 수용액을 dropping funnel을 사용하여 온도를 유지하며 4시간 동안 떨어뜨린다. 다 떨어진 후에는 상온에서 12시간가량 식힌 후, 생성된 노란색 고체를 methyl alcohol과 증류수를 사용하여 수세하고, 진공오븐을 사용해 60oC에서 8시간 이상 충분히 건조시켜 여분의 용매를 모두 제거한다[32].
2.3 BPH의 합성
Pyrazine 1.6 g, benzyl bromide 7.3 g를 500 ml 3구 플라스크에 넣고 상온에서 24시간 마그네틱 바를 사용하여 교반시킨다. 24시간 이후에 생성된 benzylpyrizinium bromide salt를 증류수에 녹인 후, 용액에 5.17 g의 NaSbF6를 첨가하고 마그네틱 바를 사용해 교반을 시켜 흰색 고체를 얻는다. 생성된 고체는 methyl alcohol을 사용하여 수세 및 재결정 후, 12시간 이상 진공 건조시켜 용매를 제거한다[33,34].
2.4 에폭시 경화
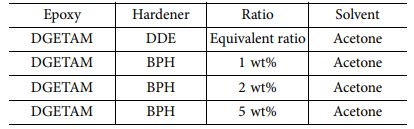
DGETAM의 경화제는 합성한 BPH 이외에 아민계 경화제인 DDE를 사용하였다. 아민계 경화제인 DDE는 반응할 수 있는 활성 수소가 말단에 4개 존재하고, DGETAM은 말단에 에폭시가 2개 존재하기 때문에 당량비는 1:2로 설정하였고, BPH는 무게비로 1, 2, 5 wt%를 사용하였다. 모든 샘플은 DGETAM 2 g을 기준으로 넣고, 용매로 acetone을 사용하여 30분 가량 소니케이터를 사용해 분산시켜준다. 분산된 용액을 테플론 디쉬에 담고 후드 안에서 12시간 이상 자연 건조하여 acetone을 제거한다. Acetone 제거 후, 막자와 막자사발을 사용하여 곱게 갈아준 후 hot press를 사용하여 180oC에서 필름 형태로 Table 1 조건으로 샘플을 제작한다.
2.5 특성 분석
2.5.1 Nucler magnetic resonance spectroscopy (NMR)
Bruker사의 Advance400을 사용하였고, DGETAM의 경우 CDCl3을 BPH는 Acetone-d6를 용매로 사용하였다.
2.5.2 Fourier transform infrared spectroscopy (FT-IR)
Bruker사의 VERTEX70을 사용하여 스캔 수 32, 600 cm-1- 4000 cm-1 범위에서 측정하였다.
2.5.3 Polarized optical microscopy (POM)
Nikon사의 OPTIOHOT-POL을 사용하였고, Hot-stage를 장착해 10oC/min의 승온 속도로 액정성을 확인했다.
2.5.4 X-ray diffraction (XRD)
샘플의 액정성을 확인하기 위해 Bruker사의 D2PHASER를 사용하여 50-60°의 범위에서 측정하였다.
2.5.5 Differential scanning calorimetry (DSC)
Perkin-Elmer사의 Diamond DSC를 사용하여 질소 기류에서 10oC/min의 승온 속도와 냉각 속도로 20-250oC의 온도범위에서 측정하였다.
2.5.6 Thermogravimetric analysis (TGA)
METTLER TOLEDO사의 DSC/TGA1을 사용하여, 질소 기류 하에 300, 310, 320, 330oC의 온도에서 50분간 등온 열분해를 진행하였다.
2.5.7 Laser flash apparatus (LFA)
NETZSCH사의 LFA 467을 사용하여 열확산계수를 측정 후, 샘플의 밀도, 비열을 이용해 열전도도를 구하였다.
3.1 DGETAM의 합성 확인
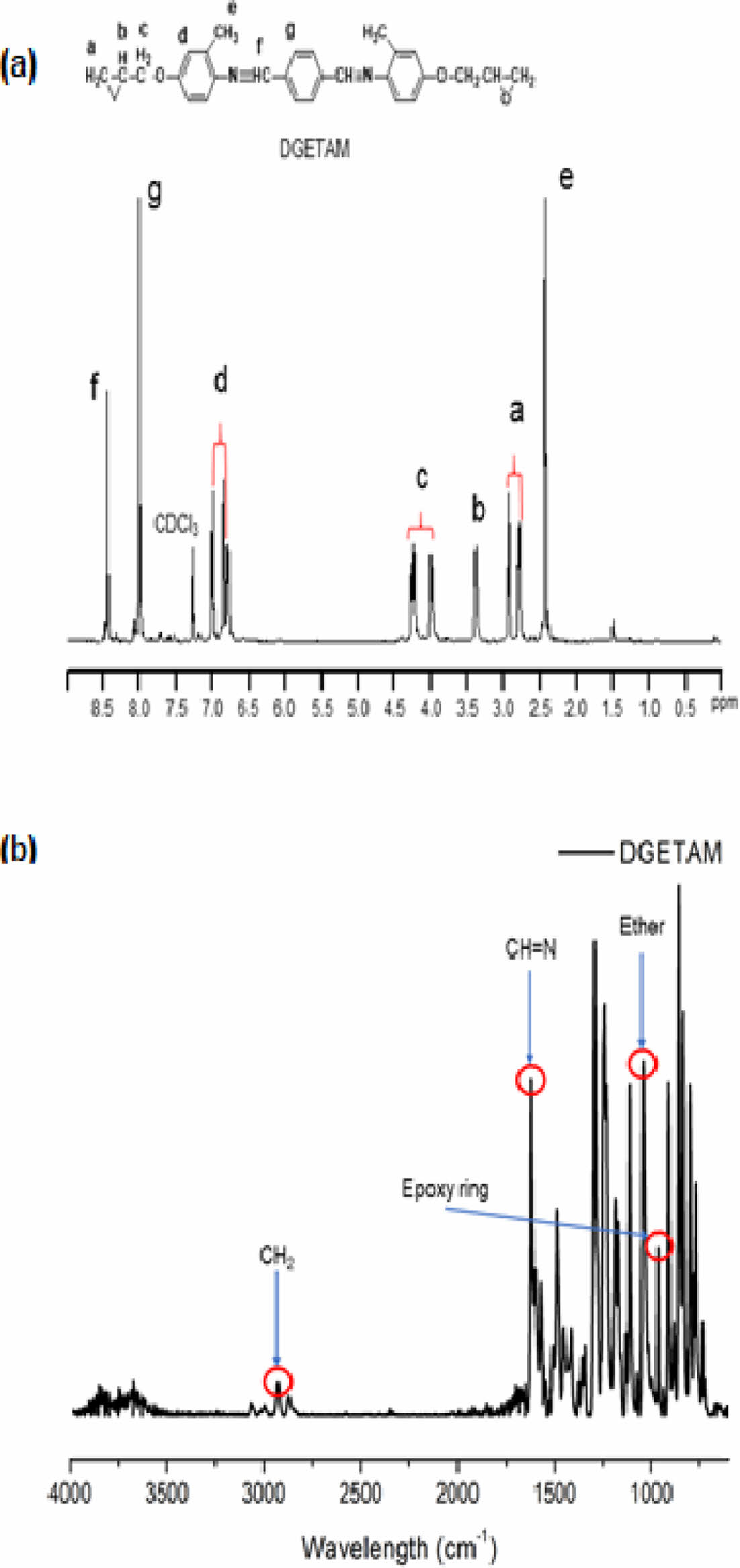
DGETAM을 합성하여 1H-NMR을 사용해 측정했을 때 에폭시 링에 관련된 a, b의 피크가 2.77-2.93, 3.36-3.38 ppm에 위치한 것을 확인할 수 있었고, 벤젠의 피크인 d, g가 6.77-7, 8 ppm에서 확인할 수 있었고 이를 Fig. 1(a)에 나타내었다. FT-IR을 사용해 측정했을 때 2900 cm-1에서 CH2 피크를, 1620 cm-1에서 CH=N 피크를, 911 cm-1에서 에폭시 링과 관련된 피크를 확인할 수 있었으며, 1040 cm-1에서 ether에 해당하는 피크를 확인할 수 있었으며 이를 Fig. 1(b)에 나타내었다.
3.2 DGETAM의 액정상 확인
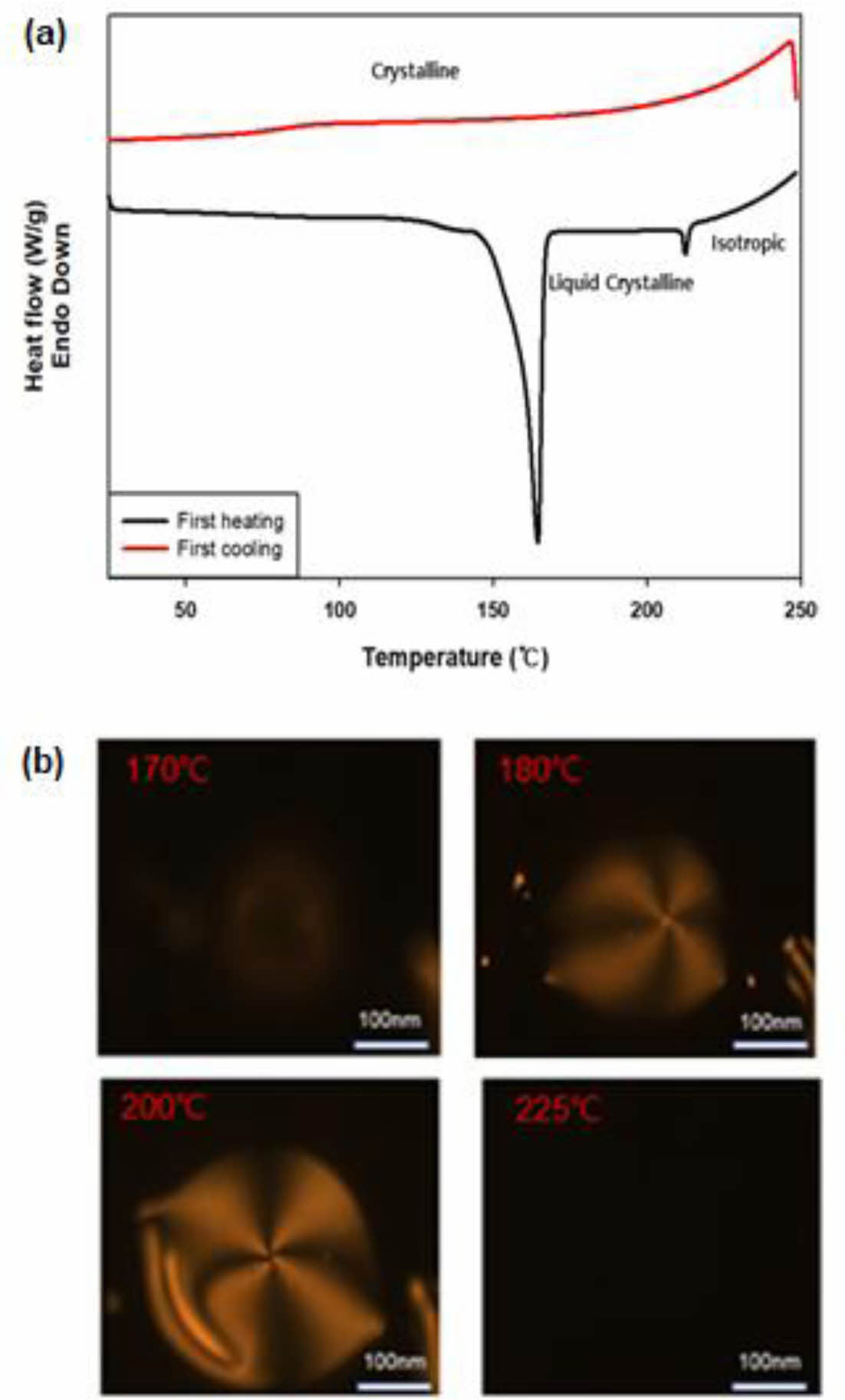
합성한 DGETAM의 액정의 형성을 확인하기 위해 DSC와 POM으로 액정이 형성되는 온도 범위와 상의 형태를 확인하였다. DSC 분석 결과 Fig. 2(a)와 같은 데이터를 얻을 수 있었다. 아래쪽 그래프에 보여진 바와 같이 가열 시 2개의 흡열 피크가 163.9oC, 212.3oC에서 나타났으며, 가열 시 최초에 생기는 큰 피크가 액정의 형성을 의미하며, 작은 피크가 액정의 소멸, 등방성을 나타내는 것을 의미한다. 위쪽 그래프에 표기된 바와 같이 냉각 시에는 245.9oC에서 발열 피크가 나타났다. 가열 시에만 액정이 나타나는 것으로 보아 단방성(monotropic) 액정임을 확인할 수 있다. POM에 hot-stage를 장착 후 10oC/min의 승온 속도로 가열한 결과 170-224oC에서 Fig. 2(b)와 같이 birefringence 무늬를 확인할 수 있었고 십자 형태의 Schlierene 무늬가 나타나는 것으로 보아 DGETAM은 네마틱 액정을 형성하는 것을 알 수 있다[35,36].
3.3 BPH의 합성 확인
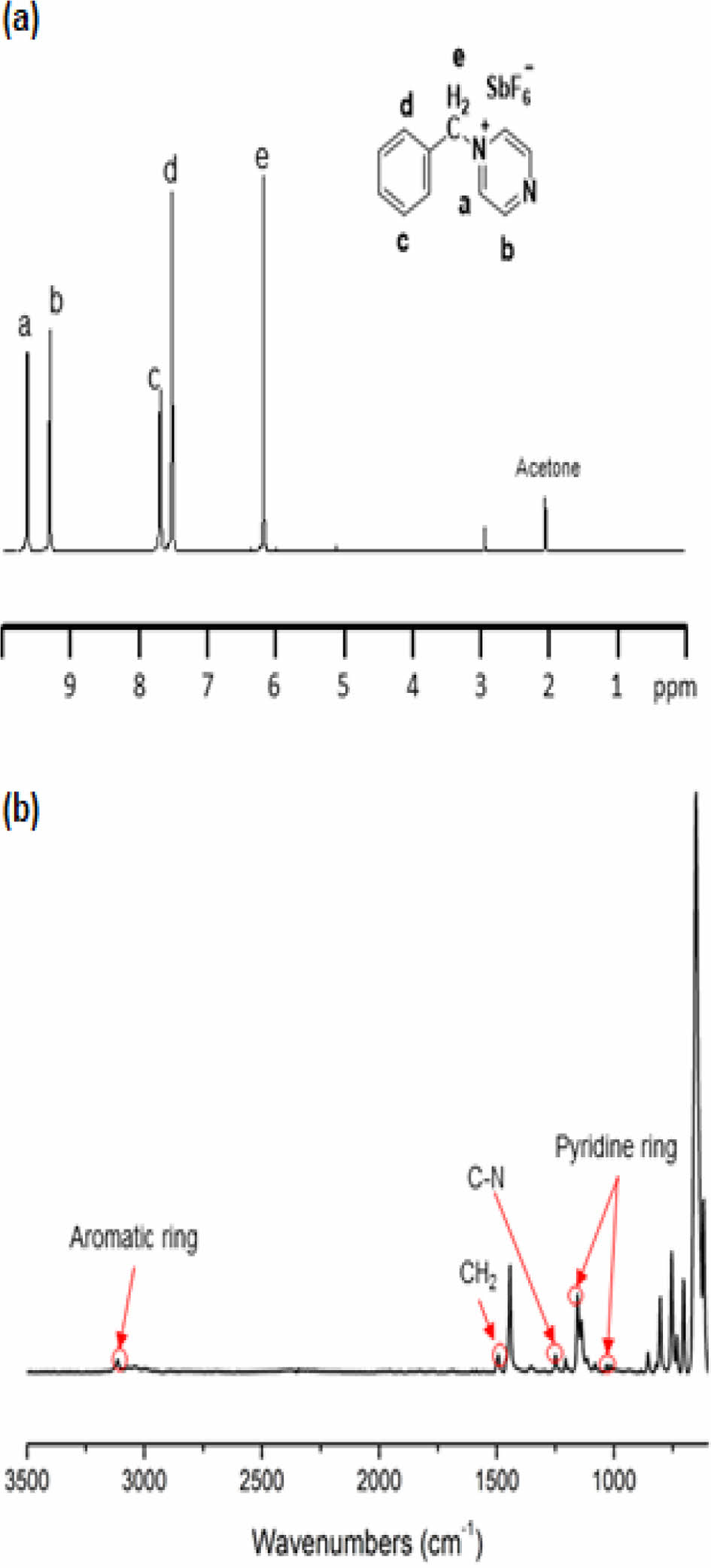
BPH를 합성하여 1H-NMR을 사용해 측정했을 때 pyridine ring의 피크인 a, b를 9.65-9.7, 9.33-9.38 ppm에 위치한 것을 확인 할 수 있었고, 벤젠의 피크인 c, d가 7.7-7.47 ppm에서 확인할 수 있었고 이를 Fig. 3(a)에 나타내었다. FT-IR을 사용해 측정했을 때 3100, 1223, 1015 cm-1에서 벤젠과 pyridine ring 피크를, 1514 cm-1에서 CH2 피크를, 911 cm-1에서 에폭시 링과 관련된 피크를 확인할 수 있었으며, 1358 cm-1에서 C-N에 해당하는 피크를 확인할 수 있었으며 이를 Fig. 3(b)에 나타내었다.
3.4 경화물의 구조 및 액정성 분석
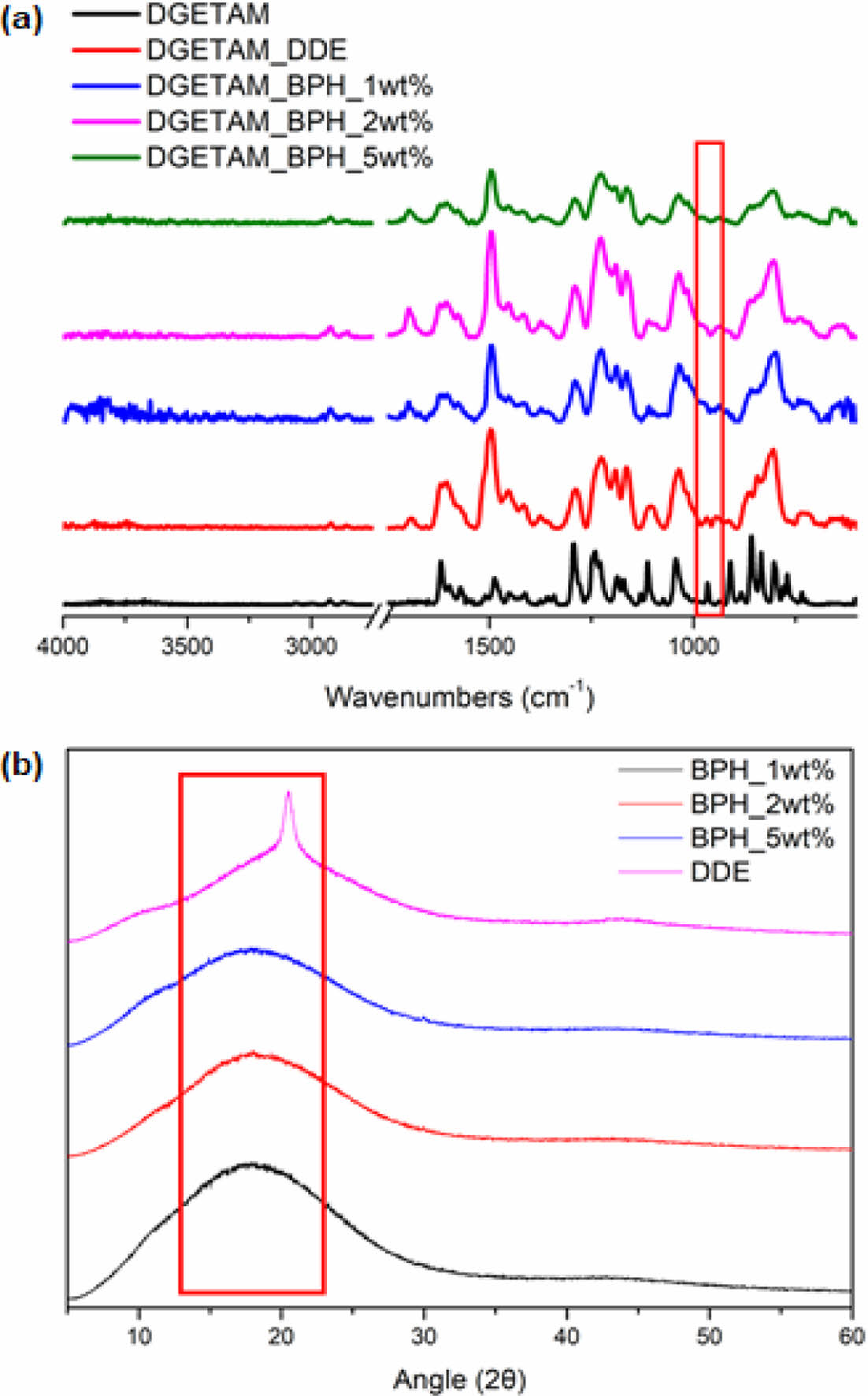
에폭시 필름의 경화가 액정을 유지하며 제대로 이뤄졌는지 확인하기 위해 FT-IR과 XRD를 이용하였는데 Fig. 4(a)에서 확인할 수 있듯이, DGETAM에서는 약 911 cm-1에서 에폭시 링과 관련된 피크를 확인할 수 있지만, 경화 후의 필름에서는 이 피크가 나타나지 않는 것으로 보아 경화가 제대로 이뤄졌음을 확인할 수 있었다. XRD 곡선 에서 네마틱 액정은 2θ=18-22° 사이에 위치한 피크로 나타나게 된다. Fig. 4(b)를 통해 해당 위치에서 피크가 존재하는 것으로 보아 제조된 에폭시 필름들이 액정을 유지한 상태로 경화가 된 것을 확인할 수 있다. 하지만 기존 연구와는 달리 BPH를 사용해 경화한 필름이 DDE를 사용한 필름보다 피크가 다소 작게 나타났다. 이는 기존 보고와는 다르게 BPH를 사용했을 때, 오히려 액정 구조 형성이 방해 받아 결정 구조가 덜 형성된 것으로 보인다.
3.5 LFA를 이용한 열전도도 분석
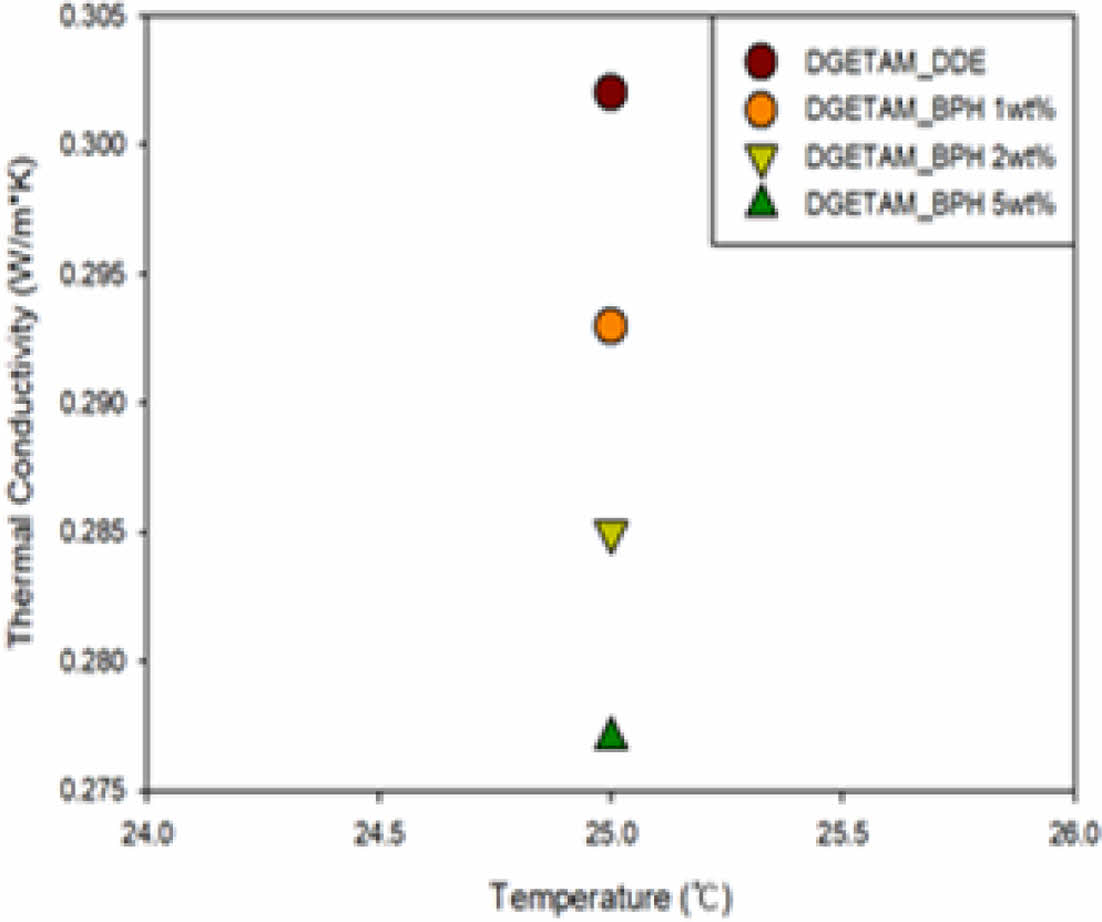
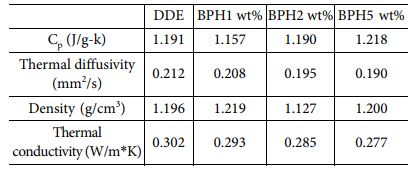
에폭시 필름의 열전도도를 분석하기 위해 LFA를 사용하였다. 열전도도는 식 (1)을 사용하여 구할 수 있고 Fig. 5에 나타내었다. 열전도도는 DDE를 사용한 경우, BPH를 사용한 경우 보다 높게 나타났으며, BPH 함량의 증가에 따라 열전도도가 떨어지는 것을 확인 할 수 있었다. 이는 Table 2의 열확산 계수가 BPH의 함량 증가에 따라 감소하는 것은, 액정의 형성에 따라 포논의 산란이 감소된다는 기존 연구와 일치하는 결과로, DGETAM_BPH 시스템에서 액정 구조 형성이 제대로 이뤄지지 않아 아민계 경화제를 사용했을 때 보다 열전도도가 감소한 것으로 보인다[37,38].
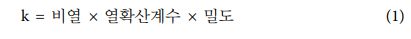
3.6 TGA를 이용한 열분해 거동 분석
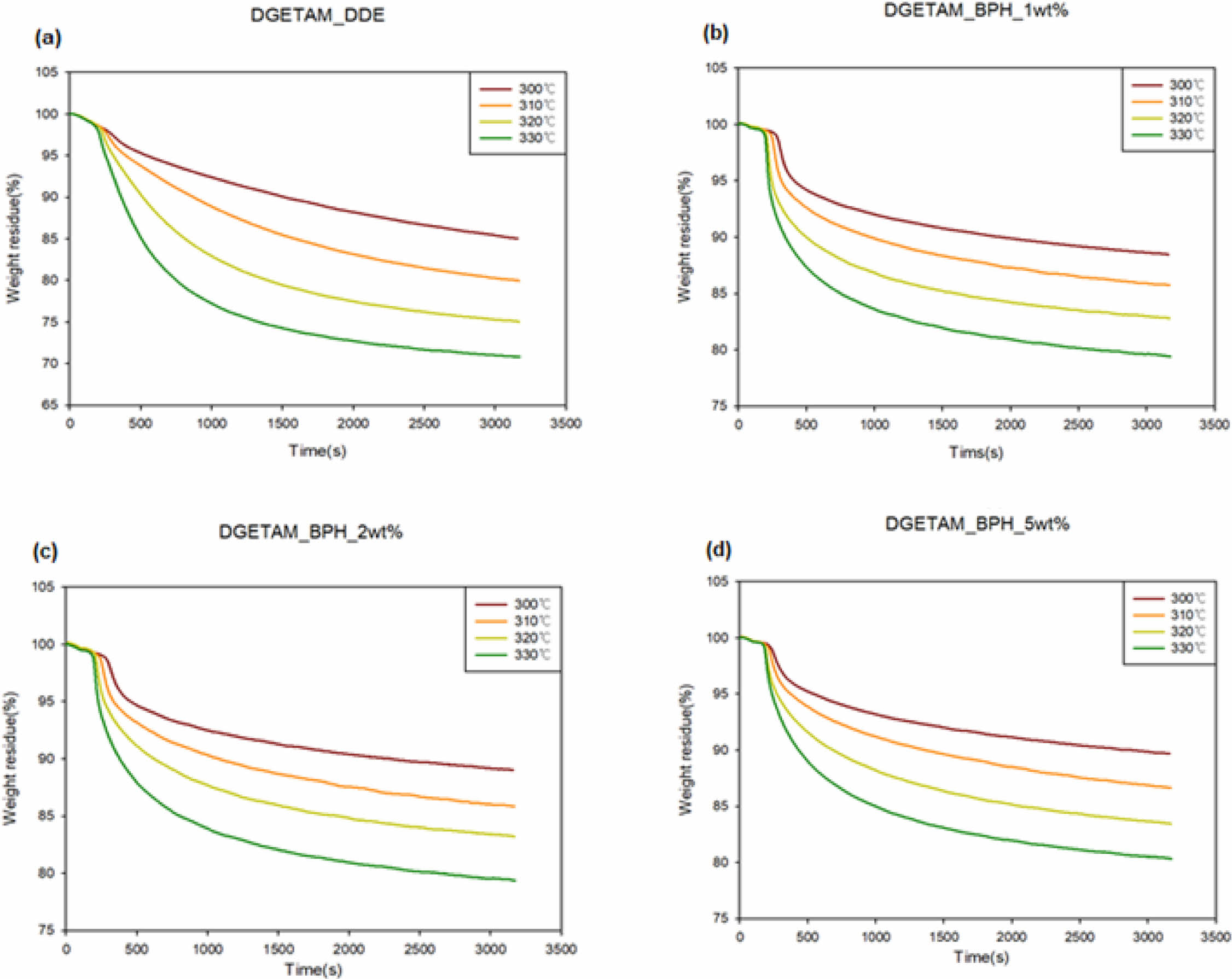
에폭시 필름의 가열에 따른 열적 성질을 확인하기 위하여 열분해 활성화 에너지를 계산하였다. 활성화 에너지를 구하기 위해 열중량 분석기(TGA)를 사용하여 샘플 당 300, 310, 320, 330oC의 온도에서 각각 50분간 등온 열분해 실험을 진행하였다. 등온 열분해 결과를 Fig. 6에 나타내었고 열분해 활성화 에너지는 식 (2)를 이용하여 계산하였다.

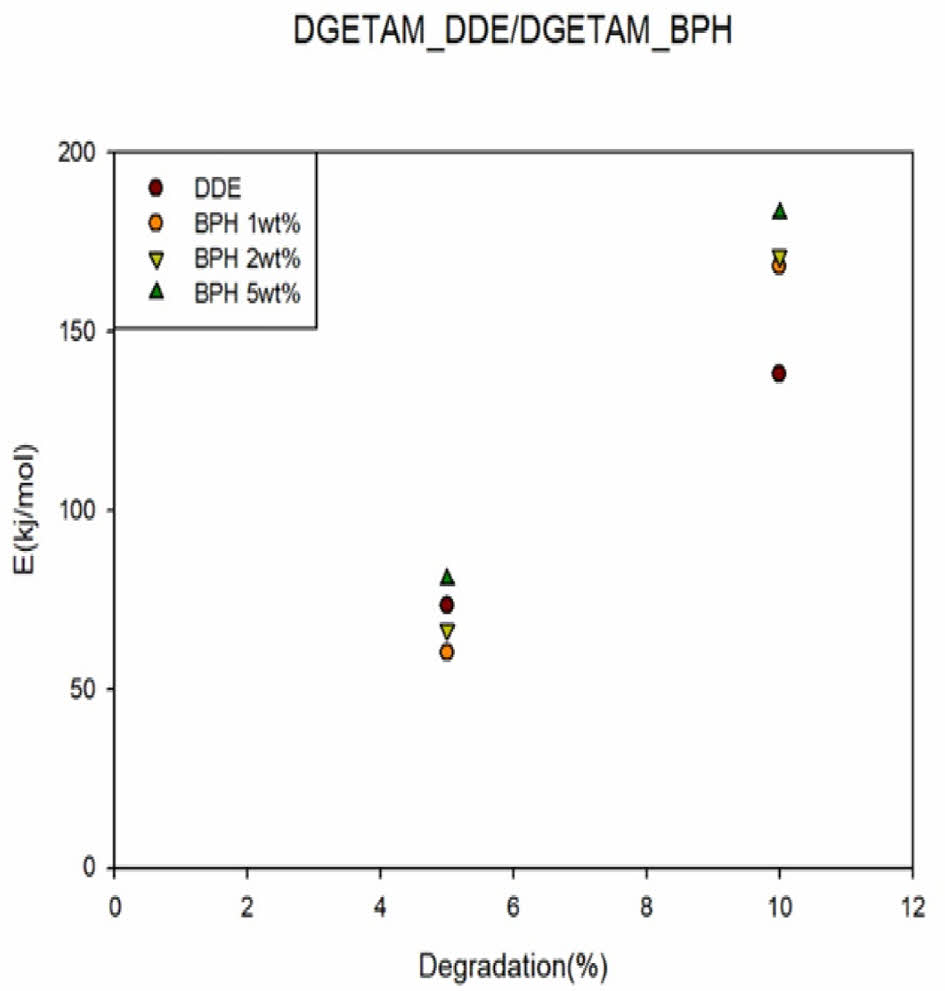
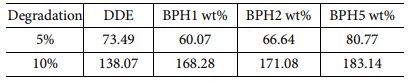
분해율 α에서의 시간 t에 대한 식을 Arrhenius 식을 적용한 후, 자연로그를 취해 나타낸 식으로 분해 반응 차수가 변하지 않을 경우 직선의 기울기를 이용해 활성화 에너지를 구할 수 있다. 에폭시를 전자재료나 패키징에 사용하기 위해서는 초기의 분해 거동이 중요하기 때문에 분해율 α가 5%, 10%인 경우에 대해 식 (2)를 이용하여 plot한 후 graph의 기울기를 이용해 계산한 열분해 활성화 에너지를 Fig. 7과 Table 3에 나타내었다. 분해율이 10%에서 전반적으로 BPH를 사용해 경화한 경우, 더 높은 활성화 에너지를 보였으나 5%에서는 DDE를 사용한 필름의 활성화 에너지와 BPH 5 wt%가 유사한 값을 나타내었다. 이는 DDE 샘플의 열전도도가 BPH 샘플의 열전도도보다 높아, 5% 분해에서는 DGETAM_DDE 샘플이 더 많은 열을 방출해 활성화 에너지가 BPH 5 wt%와 유사하게 나타난 것으로 보인다. 10 wt%에서는 방열의 한계로 CH2-O-CH2 결합의 bond dissociation energy가 335 kJ/mol인데 비해 CH3-N(CH3)C6H5의 bond dissociation energy가 272 kJ/mol로 더 낮아 DDE를 사용한 필름이 더 낮은 활성화 에너지를 나타낸 것으로 보인다.
|
Fig. 1 DGETAM (a) 1H-NMR and (b) FT-IR data |
|
Fig. 2 DGETAM (a) DSC and (b) POM data |
|
Fig. 3 BPH (a) 1H-NMR and (b) FT-IR data |
|
Fig. 4 (a) FT-IR data of DGETAM, DDE, BPH 1,2,5 wt%, (b) XRD data of DGETAM_BPH and DDE |
|
Fig. 5 LFA data of epoxy film thermal conductivity |
|
Fig. 6 Isothermal TGA graph (a)DDE, (b) BPH 1 wt%, (c) BPH 2 wt%, (d) BPH 5 wt% |
|
Fig. 7 Activation energy of DGETAM_DDE and DGETAM_BPH |
본 연구에서는 낮은 점도와 높은 열전도도를 갖는 액정 에폭시 DGETAM과 양이온 개시제인 BPH를 합성하고, 아민계 경화제인 DDE를 사용한 경우와 비교해 경화구조에 따른 열적 물성의 차이를 알아보고자 하였다. DGETAM은 DSC와 POM을 통해 네마틱 액정을 형성하는 것을 확인할 수 있었다. 액정 구조가 형성되는 온도에서 BPH와 DDE를 사용하여 에폭시 필름을 제조하였고, 제조한 필름의 열전도도를 확인하기 위해 LFA를 사용하였고, 열적 안정성을 확인하기 위해 TGA를 사용하여 열분해 활성화 에너지를 구하였다. 측정 결과 BPH를 사용한 경우, DDE를 사용해 경화한 필름 대비 열전도도가 오히려 떨어지는 것을 확인 할 수 있었으나, 열분해 활성화 에너지는 오히려 증가하는 것을 확인할 수 있었다. 이는 BPH를 사용해 경화를 진행할 경우에 액정 구조의 형성에 방해가 되어 열전도도가 감소하였지만, bond dissociation energy의 차이로 인해 열적 안정성은 증가한 것으로 보인다. 또한 초기 열분해 과정에서는 상대적으로 높은 열전도도를 보이는 DGETAM_DDE 필름이 BPH 5 wt%와 유사한 활성화 에너지를 나타내는 것으로 보아, 열전도도의 증가가 열적 안정성에 영향을 주는 것을 확인할 수 있었다.
본 연구는 한국연구재단의 기초과학연구 프로그램 지원으로 수행되었습니다(NRF-2018R1A2B60004512).
- 1. Hwangbo, S., and Cho, S.H., “Thermal Decomposition Behavior of LCT Composites Using Boron Nitride Filler,” Textile Science and Engineering, Vol. 55, No. 1, 2018, pp. 35-40.
-

- 2. Tanaka, S., Hojo, F., Takezawa, Y., Kanie, K., and Muramatsu, A., “Highly Oriented Liquid Crystalline Epoxy Film: Robust High Thermal-Conductive Ability,” ACS Omega, Vol. 3, No. 3, 2018, pp. 3562-3570.
-

- 3. Fu, Y.X., He, Z.X., Mo, D.C., and Lu, S.S., “Thermal Conductivity Enhancement with Different Fillers for Epoxy Resin Adhesives,” Applied Thermal Engineering, Vol. 66, No. 1-2, 2014, pp. 493-498.
-

- 4. Bhattacharya, S.K., and Tummala, R.R., “Integral Passives for Next Generation of Electronic Packaging: Application of Epoxy/Ceramic Nanocomposites as Integral Capacitors,” Microelctronics Journal, Vol. 32, No. 1, 2001, pp. 11-19.
-

- 5. Liang, Y., Zhang, J., Li, M., Guo, Y., and Yuan, J., “Thermal Analysis of the Heat Exchanger for Power Electronic Device with Higher Power Density,” Przeglad Elektrotechniczny, Vol. 18, No. 12, 2012, pp. 328-332.
- 6. Yun, C.S., Malberti, P., Ciappa, M., and Fichtner, W., “Thermal Component Model for Electrothermal Analysis of IGBT Module Systems,” IEEE Transactions on Advanced Packaging, Vol. 24, No. 3, 2001, pp. 401-406.
-

- 7. Prasher, R., “Thermal Interface Materials: Historical Perspective, Status, and Future Directions,” Proceedings of the IEEE, Vol. 94, No. 8, 2006, pp. 1571-1586.
-

- 8. Jo, H.S., Kang, H.Y., and Lee, G.W., “Measurement and Evaluation of Thermal Expansion Coefficients of Micrometer-sized SiO2 Particle-reinforced Epoxy Composites,” Transactions of the Koreans Society of Mechanical Engineers, Vol. 39, No. 2, 2015, pp. 129-135.
-

- 9. Fang, L., Wu, C., Qian, R., Xie, L., Yang, K., and Jiang, P., “Nano-micro Structure of Functionalized Boron Nitride and Aluminum Oxide for Epoxy Composites with Enhanced Conductivity and Breakdown Strength,” RSC Advances, Vol. 4, No. 40, 2014, pp. 21010-21017.
-

- 10. Lu, D., and Wong, C.P., Materials for Advanced Packaging, Springer, 2nd ed, 2017, pp. 28-31.
- 11. Moon, H.J., Kim, K.H., Hwangbo, S., and Cho, S.H., “Thermal Decomposition Activation Energy of Liquid Crystalline Epoxy Composite with Zirconia Filler,” Textile Science and Engineering, Vol. 52, No. 3, 2015, pp. 206-214.
-

- 12. Ku, M.Y., Kim, J.H., Kang, H.Y., and Lee, G.W., “Measurement of Mechanical Property and Thermal Expansion Coefficient of Carbon-Nanotube-Reinforced Epoxy Composites,” Transactions of the Korean Society of Mechanical Engineers, Vol. 37, No. 5, 2013, pp. 657-664.
-

- 13. Heo, G.Y., and Rhee, H.Y., “Influence of Alkylation on Interface and Thermal Conductivity of Multi-walled Carbon Nanotubes-reinforced Epoxy Resin,” Polymer, Vol. 35, No. 6, 2011, pp. 548-552.
- 14. Choi, J.R., and Park, S.J., “A Study on Thermal Conductivity and Fracture Toughness of Alumina Nanofibers and Powders-filled Epoxy Matrix Composites”, Polymer(Korea), Vol. 37, No. 1, 2013, pp. 47-51.
-

- 15. Burger, N., Laachachi, A., Ferriol, M., Lutz, M., Toniazzo, V., and Ruch, D., “Reviews of Thermal Conductivity in Composites: Mechanisms, Parameters and Theory,” Progress in Polymer Science, Vol. 61, 2016, pp. 1-28.
-

- 16. Wang, F., Drzal, L.T., Qin, Y., and Huang, Z., “Mechanical Properties and Thermal Conductivity of Graphene Nanoplatelet/epoxy Composites,” Journal of Materials Science, Vol. 50, No. 3, 2015, pp. 1082-1093.
-

- 17. Kim, B.A., and Moon, C.K., “Effect of TiO2 Particle Size and Content on the Mechanical Properties of TiO2/Epoxy Composites,” Journal of the Korean Society for power System Engineering, Vol. 21, No. 1, 2017, pp. 11-17.
-

- 18. Lee, J.Y., Shim, M.J., and Kim, S.W., “Synthesis of Liquid Crystalline Epoxy and Its Mechanical and Electrical Characteristics-Curing Reaction of LCE with Diamines by DSC Analysis,” Journal of Applied Polymer Science, Vol. 83, No. 11, 2002, pp. 2419-2425.
-

- 19. Kim, Y.C., Orh, J.B., and Lee, B.J., “Synthesis and Characterization of Liquid Crystalline Epoxy Acrylate,” Journal of Korean Industrial and Engineering Chemistry, Vol. 13, No. 6, 2002, pp. 538-543.
- 20. Song, T., Li, Z., Kiu, J., and Yang, S., “Synthesis, Characterization and Properties of Novel Crystalline Epoxy Resin with Good Melt Flowability and Flame Retardancy Based on an Asymmetrical Biphenyl Unit,” Polymer Science, Ser. B., Vol. 55, No. 3-4, 2013, pp. 147-157.
-

- 21. Su, W.F.A., Chen, K.C., and Tseng, S.Y., “Effects of Chemical Structure Changes on Thermal Mechanical, and Crystalline Properties of Rigid Rod Epoxy Resins,” Journal of Applied Polymer, Vol. 78, No. 2, 2000, pp. 446-451.
-

- 22. Li, Y., Badrinarayanan, P., and Kessler, M.R., “Liquid Crystalline Epoxy Resin Based on Biphenyl Mesogen: Thermal Characterization,” Polymer, Vol. 54, No. 12, 2013, pp. 3017-3025.
-

- 23. Young, R.J., and Lovell, P.A., Introduction to Polymers,” Journal of the Korean Society for Composite Materials, CRC Press, 3rd Ed., 2011.
-

- 24. Donald, A.M., Windle, A.H., and Hanna, S., Liquid Crystalline Polymers, Cambridge, 2nd Ed., 2006.
-

- 25. Blumstein, A., Liquid Crystalline Order in Polymers, Elsevier Science, 2015.
- 26. Harada, M., Hamaura, N., Ochi M., and Agari, Y., “Thermal Conductivity of Liquid Crystalline Epoxy/BN Filler Composites Having ordered Network Structure,” Composites Part B, Vol. 55, 2013, pp. 306-313.
-

- 27. Kim, Y., Jung, J., Yeo, H., You, N., Jang, S. G., Ahn, S., Lee, S.H., and Goh, M.J., “Development of Highly Thermal Conductive Liquid Crystalline Epoxy Resins for High Thermal Dissipation Composites,” Composites Research, Vol. 30, No. 1, 2017, pp. 1-6.
-

- 28. Park, S.J., Kim, H.C., Lee, H.I., and Suh, D.H, “Thermal Stability of Imidized Epoxy Blends Initiated by N-Benzylpyrazinium Hexafluoroantimonate Salt,” Macromolecules, Vol. 34, No. 22, 2001, pp. 7573-7575.
-

- 29. Islal, A.M., Lim, H., You, N.H., Ahn, S., Goh, M., Hahn, J.R., Yeo, H., and Jang, S.G., “Enhanced Thermal Conductivity of Liquid Crystalline Epoxy Resin using Controlled Linear Polymerization,” ACS Macro Letters, Vol. 7, No. 10, 2018, pp. 1180-1185.
-

- 30. Jung, Y.J., Hyun, H.N., and Cho, S.H., “Thermal Decomposition Activation Energy of Liquid Crystalline Epoxy using Cationic Initiator,” Composites Research, Vol. 34, No. 3, 2021, pp. 180-185.
- 31. Pascault, J.P., Sautereau, H., Verdu, J., and Williams, R.J.J., Thermosetting Polymers, CRC Press, 1st Ed., 2002.
-

- 32. Harada, M., Ochi, M., Tobita, M., Kimura, T., Ishigaki, T., Shimoyama, N., and Aoki, H., “Thermomechanical Properties of Liquid-crystalline Epoxy Networks Arranged by a Magnetic Field,” Journal of Polymer Science: Part B: Polymer Physics, Vol. 42, No. 5, 2004, pp. 758-765.
- 33. Lee, S.H., Kim, J.I., Park, C.S., Lee, S.B., Kim, J.H., and Kim, M.S., “Preparation of Intercross-linked Poly(L-lactide) and Epoxy Resin Using N-benzyl Pyrazine Hexafluoroantimonate,” Journal of Polylmer Research, Vol. 20, No. 11, 2013, pp. 1-6.
-

- 34. Kim, Y.C., Park, S.J., and Lee, J.R., “Effects of N-Benzylpyrazinium Hexafluoroantimonate Concentration on Rheological Properties in Cationic Epoxy Cure System,” Polymer Journal, Vol. 29, No. 9, 1997, pp. 759-765.
- 35. Madsen, L.A., Dingemans, T.J., Nakata, M., and Samulski, E.T., “Thermotropic Biaxial Nematic Liquid Crystals,” Physical Revies Letters, Vol. 92, No. 14, 2004, pp. 145505.
-

- 36. Lin, Q., Yee, A.F., Earls, J.D., Hefner Jr, R.E., and Sue, H.J., “Phase Transformations of a Liquid Crystalline Epoxy during Curing,” Polymer, Vol. 35, No. 12, 1994, pp. 2679-2682.
-

- 37. Park, Y.B., Yang, H.J., Kweon, J.H., Choi, J.H., and Cho, H.I., “Flash Method of Determining Thermal Diffusivity, Heat Capacity, and Thermal Conductivity,” Journal of Applied Physics, Vol. 32, No. 9, 1961, pp. 1679-1684.
-

- 38. Wen, S., Liu, Y., Kaptay, G., and Du, Y., “A New Model to Describe Composition and Temperature Dependence of Thermal Conductivity for Solution Phases in Binary Alloys,” Journal of Materials Science & Technology, Vol. 59, 2020, pp. 72-82.
-

 This Article
This Article
-
2022; 35(2): 53-60
Published on Apr 30, 2022
- 10.7234/composres.2022.35.2.053
- Received on Nov 18, 2021
- Revised on Feb 10, 2022
- Accepted on Mar 20, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Seung-Hyun Cho
-
Department of Organic Materials and Fiber Engineering, Soong-sil University
- E-mail: scho@ssu.ac.kr






 Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.
Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.