- Non-Woody Biomass-Derived Materials for Tissue Engineering and Orthopedic Applications
Hui-Yun Hwang†
School of Electronics and Mechanical Engineering, Gyeongkuk National University
- 비목질계 바이오매스 유래 소재의 조직공학 및 정형외과적 응용
황희윤†
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
This paper analyzed the anatomical and chemical characteristics of non-woody plant resources such as flax, hemp, and ramie, and reviewed the latest research trends in their applications as tissue engineering and orthopedic medical materials. Non-woody resources offer advantages such as short growth cycles and the potential for low-carbon model implementation. The high-strength bast fibers and porous pith constituting the stems of non-lignified plant resources are utilized for their mechanical structural properties and as scaffolds for cell growth. Notably, composite materials based on non-lignified bast fibers can achieve elastic moduli similar to human cortical bone, thereby resolving the stress shielding phenomenon associated with metallic implants. Furthermore, the core components of non-lignified plant resources—cellulose, hemicellulose, and lignin—possess excellent biocompatibility, antioxidant, and antibacterial properties. This has confirmed their utility across diverse biomedical engineering fields, including bone regeneration scaffolds, customizable 3D bioprinting inks, biodegradable orthopedic fixation devices, and dental barrier membranes.
본 논문은 아마, 헴프, 양마 등의 비목질계 식물 자원의 해부학적∙화학적 특성을 분석하고, 이를 조직공학 및 정형외과용 의료 소재로 응용한 최신 연구 동향을 고찰하였다. 비목질계 자원은 생육 주기가 짧고 저탄소 모델 구현이 가능하다는 장점이 있다. 비목질계 식물 자원의 줄기를 구성하는 고강도 인피섬유와 다공성 속대는 구조의 기계적 특성과 세포 성장을 위한 지지체로 활용된다. 특히, 비목질계 인피 섬유 기반 복합재료는 인체 피질골과 유사한 탄성계수를 구현할 수 있어, 금속 장치가 가지는 응력 차폐 현상을 해결할 수 있다. 또한, 비목질계 식물 자원의 핵심 성분인 셀룰로오스, 헤미셀룰로오스, 리그닌은 우수한 생체 적합성, 항산화 및 항균 특성을 가지고 있어, 골 재생 지지체, 맞춤형 3D 바이오 프린팅 잉크, 정형외과용 생분해성 고정 장치 및 치과용 차단막 등 다양한 의공학 분야에 활용되고 있음을 확인하였다.
Keywords: 비목질계(Non-woody), 인피 섬유(Bast fibers), 속대(Hurds), 골조직공학(Bone tissue engineering), 정형외과용 임플란트(Orthopedic implants)
1.1 의공학 분야 내 지속 가능한 바이오 소재의 필요성
조직 재생이나 정형외과 분에 활용되는 금속 보철재는 생체 내 응력 차폐(Stress shielding) 현상을 일으켜 주변 골 조직의 악화를 초래한다[1]. 합성 고분자 재료는 분해 시 산성 부산물을 생성하여 조직 내 염증을 유발하거나, 화석 연료 기반 생산 공정으로 인해 환경 문제를 야기하고 있다.
이에 비해, 비목질계 천연 소재를 구성하고 있는 셀룰로오스(Cellulose), 헤미셀룰로오스(Hemicellulose), 리그닌(Lignin) 등의 성분은 다량의 수산기(Hydroxyl group, -OH)를 보유하여 화학적 수식이 용이하며, 생체 조직 내 세포 부착 및 증식을 활성화하는 구조적 토대를 마련할 수 있다[3]. 특히, 나노 단위로 분리된 셀룰로오스는 인체 콜라겐(Collagen) 섬유와 유사한 나노 네트워크를 형성하여 기계적 강도와 생체 적합성을 동시에 만족하는 지지체를 구현할 수 있다[4]. 또한, 헴프(Hemp), 아마(Flax), 양마(Kenaf), 황마(Jute)와 같은 비목질계 자원은 목재 대비 짧은 생육 주기를 나타내며, 경작 과정에서의 탄소 흡수 능력이 탁월하여 저탄소 바이오 복합재료 생산에 적합하다[5]. 따라서, 농업 부산물을 고부가가치 의료용 소재로 재자원화하는 공정은 폐기물 발생을 최소화하고 자원 순환을 극대화하는 ‘Garbage In Biomaterials Out (GIBO)’ 모델의 핵심적 기술로 고려된다[6].
1.2 목질계 자원 대비 비목질계 천연 소재의 우위성
수십 년의 성장 기간이 소요되는 목질계 자원과 달리, 헴프, 아마, 양마 등은 연간 수확이 가능한 단기 생육 주기를 나타내어 원료의 안정적 수급이 용이하다[7]. 또한, 단위 면적당 바이오매스(Biomass) 생산량이 목재 대비 우수하며, 경작 과정에서 비료 및 살충제 사용량이 적어 의료용 원료로서 고순도 정제가 유리한 특성을 가진다[8].
비목질계 섬유는 목재에 비해 리그닌 함량이 낮고 셀룰로오스 비율이 높아, 상대적으로 완만한 화학 처리 공정만으로도 고결정성 나노셀룰로오스 분리가 가능하며[9], 미세섬유각(Microfibrillar angle, MFA)이 작아 축 방향의 인장 강도와 탄성 계수가 목질계 섬유보다 우수하기 때문에 하중 지지가 필요한 정형외과용 복합재료(Orthopedic Composite Materials)의 보강재로서 충분한 특성을 가진다[10]. 그리고, 식물 종에 따라 분자 사슬의 배열 및 기공 구조가 상이하여, 목적하는 생체 조직의 물성에 최적화된 소재 선택 및 설계의 유연성이 확보될 수 있다[11].
추출 및 공정 효율성 측면에서는 리그닌과 헤미셀룰로오스의 결합 구조가 목질계보다 느슨하여 나노 단위의 섬유 추출 시 에너지 소비량이 적고, 섬유의 손상을 최소화하면서도 높은 종횡비(Aspect ratio)를 유지할 수 있다[12].
1.3 논문의 목적과 범위
본 논문에서는 비목질계 자원의 핵심 성분인 셀룰로오스, 헤미셀룰로오스, 리그닌의 화학적 구조에 기계적·생물학적 기능을 연계하여 의공학적 활용 가능성을 분석하고, Table 1과 같이 각 성분별 조직공학 지지체(Tissue engineering scaffold), 상처 치유 드레싱(Wound Healing Dressing), 약물 전달체(Drug delivery system) 및 정형외과용 복합재료의 성능에 미치는 영향을 중심으로 선행 연구 결과를 종합적으로 분석하고자 한다[2,3,8,13,14].
|
Table 1 Summary of core properties and biomedical application fields of non-woody biomass components |

2.1 주요 비목질계 식물 자원의 분류 및 물리적 특성
비목질계 자원(Non-wood resources)은 목재를 제외한 식물의 줄기, 잎, 종자, 과일 등에서 확보 가능한 천연 유기 자원을 의미하는데, 식물학적 추출 부위에 따라 인피 섬유(Bast fibers), 잎 섬유(Leaf fibers), 종자/과일 섬유(Seed/Fruit fibers), 그리고 농업 부산물(Straw/Stalks/Hurds)로 나눌 수 있다. 의공학용 복합재료의 보강재로 주로 활용되는 아마, 헴프, 황마, 양마 등은 인피 식물에 해당하며, 인피 식물의 줄기는 외곽의 인피 섬유 층과 내측의 목질화된 속대 조직이 동심원 구조를 이루고 있다. 줄기 전체에서 인피섬유는 질량 기준으로 25~35%를 차지하며 식물의 인장 하중을 분산하는 역할을 담당하고, 나머지 65~75%를 차지하는 속대는 압축 하중 지지 및 수분 저장 기능을 담당하여 식물 해부학적으로 다른 물리적 특성을 가진다[9,15]. 마 기반 비목질계 식물 자원으로부터 인피 섬유와 속대의 분리 과정 (스커칭 공정)에서 발생하는 물리/기계적 특성의 차이는 각각 보철용 보강재와 다공성 조직공학 지지체로 의공학적 응용이 나뉘게 된다[12,15].
비목질계 식물 섬유의 밀도는 1.2~1.6 g/cm3 수준으로, 기존 금속 생체 소재인 티타늄(약 4.5 g/cm3)이나 스테인리스강(약 7.9 g/cm3) 뿐만 아니라 유리섬유(E-glass, ~2.5 g/cm3)에 비해서도 현저히 낮다[16]. 하나의 인피 섬유 다발(Bundle)은 여러 개의 단위 섬유(Elementary fibers)가 펙틴과 리그닌으로 구성된 중간층(Middle lamella)에 의해 결합된 형태로, 인피 섬유 강화 복합재료의 파손이 발생할 때 에너지 흡수의 중요한 역할을 하게 된다[10,12]. 단위 섬유는 여러 층의 세포벽이 동심 기둥 형태를 가지는데, 단위 섬유 내 2차 벽인 S2 층은 전체 세포벽 두께의 80% 이상을 차지하며 이 층의 미세섬유 각도(Microfibriller angle, MFA)는 섬유의 탄성 계수에 직접적인 영향을 주게 된다[10,16]. 아마와 헴프의 인피 섬유의 경우 10o 미만의 낮은 MFA를 가져, 인체 피질골의 강성보다 높은 역학적 성능을 보이며, 금속 소재 대비 인체 조직에 최적화된 비강성을 구현할 수 있는 근거가 된다[16,17].
이에 비해 속대 조직은 인피 섬유 대비 매우 낮은 밀도 (0.12~0.25 g/cm3)를 보이는데, 이는 속대가 가진 다공성 구조에 기인한다. 속대의 미세 기공(Micro-pores)는 세포의 내생(In-growth)과 영양분의 확산이 용이한 기하학적 특성이라 할 수 있다[15,18].
따라서, 인피 섬유의 높은 종횡비와 속대의 다공성 구조를 함께 활용할 경우, 소재의 밀도와 역학적 특성을 효과적으로 제어할 수 있어 맞춤형 생체 조직 설계가 가능하다[19, 20]. Table 2에 보이는 것과 같이 아마와 헴프 인피 섬유는 금속 소재에 가까운 비강성(Specific stiffness)을, 유리 섬유(Glass fiber)와 견줄 만한 비강도(Specific strength)를 보유하여 구조적 보강재로서 활용도가 높다[17]. 아마와 헴프 등을 복합재료로 제작하였을 때 탄성계수(Young’s Modulus)는 20~80 GPa 범위를 형성하여, 인체 피질골(Cortical bone, 7~30 GPa)의 물성과 유사한 거동을 나타낸다. 이러한 물성 매칭은 고강성 금속 보철재가 뼈가 받아야 할 하중을 대신 감당하여 뼈를 약화시키는 응력 차폐 부작용을 완화하고 골 융합을 촉진할 수 있다[19].
2.2 마 기반 비목질계 자원 핵심 성분의 기능성
마 기반 비목질계 자원의 핵심 성분은 셀룰로오스, 헤미셀룰로오스와 리그닌이며, 마 종류에 따라 각 성분의 함량이 달라지게 된다.
가장 많은 함량을 가지는 성분은 셀룰로오스이다. 셀룰로오스는 β-1,4-D-Glucopyranose 단위체가 글루코사이드(Glucoside) 결합으로 연결된 선형 고분자로, 인피 식물 세포벽 내에서 고결정성 미세원섬유 (Microfibrils) 구조를 형성한다[3,7]. 분자 사슬 사이의 강력한 수소 결합으로 수백 MPa 수준의 인장 강도를 가질 수 있어, 하중 지지가 필요한 골 조직 재생용 지지체로 활용할 수 있다[8,21]. 셀룰로오스를 다양한 방법으로 처리하면 나노 단위로 분리된 셀룰로오스 나노 결정(Cellulose Nanocrystals, CNC)과 나노 섬유(Cellulose Nan-fibers, CNF)를 얻을 수 있는데, 나노 셀룰로오스가 가지고 있는 수산기는 세포 부착 단백질과의 친화도를 높이는 작용을 한다[16,22].
헤미셀룰로오스는 인피 섬유 내에서 셀롤로오스와 리그닌 사이의 접착제 역할을 수행한다. 자일로스, 만노스, 글루코스 등 다양한 당류가 불규칙한 분지형 사슬을 형성하는 비결정성 다당류로, 구조적 특성으로 인해 수분 흡수 및 팽윤 능력이 우수하다[3,8]. 이러한 친수성 때문에 가교 공정을 거쳐 인체 조직과 유사한 탄성 계수를 갖는 생체 적합 하이드로젤(Hydrogels)로 활용이 가능하다. 또한, 헤미셀룰로오스 분자 내 카르복실기(Carboxyl group, -COOH)는 수화 층을 형성하여 외부 자극에 반응하여 약물 방출 속도를 조절하는 지능형 전달체 역할도 할 수 있다[3,23].
리그닌은 p-쿠마릴(Paracoumaryl), 코니페릴(Coniferyl), 시나필(Sinapyl) 알코올 등 페놀계 전구체의 무작위 라디칼 중합으로 형성된 3차원 그물망 구조를 가져, 세포벽 내에서 강성을 부여하는 충진재 역할을 한다[2,14]. 분자 내 페놀성 수산기와 메톡실기(Methoxy group, -OCH3)는 활성 산소를 제거하는 천연 항산화 기능을 가지고 있어, 세포 재생에 적합한 미세 환경을 조성할 수 있다. 또한, 소수성 방향족 고리 구조와 작용기는 병원성 미생물의 세포막 파괴를 유도하여 내재적 항균 작용을 할 수 있다[14,24]. 바이오 복합재료로 제작될 때는 단백질 가교제나 자외선 차단제 역할을 할 수 있어, 물리적/생물학적 안정성을 동시에 확보할 수 있는 다기능성 소재로 분류된다[24,25].
|
Table 2 Summary of core properties and biomedical application fields of non-woody biomass components |

3.1 생체 적합성(Biocompatibility) 및 세포 독성(Cytotoxicity)
인체 삽입형 소재로서 비목질계 천연 소재의 생체 적합성은 조직 재생 과정에서 발생할 수 잇는 국소 및 전신 면역 반응의 부재로 정의할 수 있다. ISO 10993 등의 규정에 따라 소재의 용출물에 의한 세포 생존율 저하 여부 검토는 의공학적 안정성 확보를 위한 필수적인 지표이다[27]. 이런 관점에서 인피 섬유의 정제 공정 수준은 생체 내 거부 반응에 직접적인 영향을 주는데, 특히 왁스나 펙틴(Pectin) 등의 비 셀룰로오스 성분의 불완전한 제거는 이물 반응을 촉진할 수 있으나, 정제된 인피 섬유는 우수한 생체 적합성을 보여준다[11,27].
속대나 인피 섬유 내 잔존 리그닌은 폴리페놀(Polyphenol) 구조로 인해 항염증 기전을 나타내며, 앞서 설명한 것과 같이 초기 산화 스트레스 억제를 통한 세포 재생에 적합한 미세환경을 만들 수 있다[2,27].
세포 독성 평가는 MTT(3-(4,5-di methyl thiazol-2-yl)-2,5-diphenyltetrazolium bromide)와 XTT(2,3-bis-(2-methoxy-4-nitro-5-sulfophenyl)-2H-tetrazolium-5-carboxanilide) 분석을 통해 이루어지는데, 비목질계 유래 나노 셀룰로오스 지지체 등의 표면에서 세포의 부착, 증식 및 정상적인 대사 활동이 유지됨이 보고되어 생물학적 유효성이 입증되었다[28, 29].
비목질계 인피 섬유와 속대의 표면 친수성과 다공성 구조는 혈액 적합성(Hemocompatibility)에 영향을 주는데, 특히 혈관 조직공학 지지체 등에 적용할 때 혈소판 부착(Platelet adhesion) 및 용혈 반응(Hemolysis) 을 억제하는 것으로 알려져 있다[30].
3.2 생분해 특성
인피 섬유의 지배적인 성분인 셀룰로오스는 고결정성 구조와 강한 분자 간 수소 결합으로 인해 체내 가수분해 및 효소 분해에 대한 높은 저항성을 가지며, 이로 인해 인공 지지체의 골격을 장기간 유지할 수 있다[2,7]. 반면, 비결정성 영역의 비중이 높은 속대 조직은 상대적으로 빠른 초기 분해 거동을 보이는데, 이는 생성된 조직이 안착할 수 잇는 공간을 확보하는데 유리하다[15].
구조적인 관점에서는, 속대의 다공성 구조와 넓은 비표면적으로 생체 내 수분 침투를 빨라지게 되어 효소의 접근성을 높이기 때문에 인공 지지체의 질량 감소 속도를 제어하는 주요 변수로 작용한다[15,28]. 반면, 인피 섬유의 종횡비 및 함량을 조절하게 되면 바이오 복합재료의 수분 흡수율을 제어할 수 있어 조직 재생 속도와 소재의 강성 저하 속도를 동기화할 수 있는 지지체 설계가 가능해진다[31].
비목질계 자원의 생분해 특성을 제어할 수 있는 또 다른 요소는 리그닌의 함량이다. 리그닌의 소수성 방향족 그물망 구조는 외부 인자의 침투를 억제하는 보호 장벽 역할을 하기 때문에, 리그닌 함량이 상대적으로 높은 속대 기반 소재의 경우 페놀계 작용기를 활용하여 가교 밀도를 조절함으로써 생분해 주기를 조절할 수 있다[2,23]. 또한, 나노 셀룰로오스와 생분해성 고분자의 하이브리드화를 통해 결정 영역의 치밀도를 조절하면, 효소 분해를 지연시키며 생체 환경 내 장기적인 안정성을 제어할 수도 있다[2,32].
3.3 기계적 특성
비목질계 천연 소재를 의공학 분야에 적용하는데 생화학적 특성과 함께 지지체의 형상 유지나 계면 결착을 위한 기계적 특성도 중요하다. 가장 중요한 기계적 특성은 인체 조직과의 기계적 정합성이다. 금속으로 제작된 지지체는 높은 탄성 계수로 인해 인체 골 조직으로 전달되어야 할 하중을 금속 지지체가 모두 전달받아 골 조직의 퇴화를 유발하는 응력 차폐 현상이 발생한다[10,33]. 그러나 아마나 헴프로 보강된 복합재료의 탄성계수는 인체 피질골의 탄성계수(10~30 GPa)과 유사하여, 뼈와 이식된 지지체 계면세어의 균일한 응력 분포를 유도하여 장기적 생체 구조적 안정성을 확보할 수 있다[33,35].
인피 섬유나 속대의 표면에는 풍부한 수산기가 존재하는데, 이는 생분해성 고분자와의 수소 결합 및 화학적 가교를 형성하여, 복합재료 내 소재 간 높은 계면 전단 강도 특성을 구현할 수 있다[33,35]. 또한 인피 섬유는 높은 종횡비를 가지므로 복합재료 내 균열 전파를 억제하고 섬유 인발 현상을 통해 파괴 인성과 충격 에너지 흡수 특성을 높일 수 있다[36,37]. 이뿐 만 아니라, 나노 셀룰로오스와 인피 섬유를 혼용한 하이브리드 보강재를 사용하게 되면, 복합재료 지지체의 굴곡 강도(Bending strength) 및 피로 한도(Endurance limit)의 향상을 가져올 수 있어, 반복적인 하중을 받는 정형외과용 고정구와 같은 분야의 내구성 확보에 도움이 된다[15,35].
4.1 골 조직 및 연골 재생을 위한 3차원 지지체
비목질계 인피 식물은 줄기 구조의 해부학적 이방성을 활용하여 골 결손 부위의 구조적 보강과 세포의 입체적 생장을 도울 수 있는 다공성 기지재(Matrix) 역할을 동시에 할 수 있다는 장점이 있다. 특히, 인피 섬유 유래 나노 셀룰로오스의 고강성 특성과 속대 조직의 천연 기공 구조는 하중 지지가 필수적인 골 재생과 미세환경 조절이 중요한 연골 재생 분야에 지지체로서 응용 사례를 분석하였다.
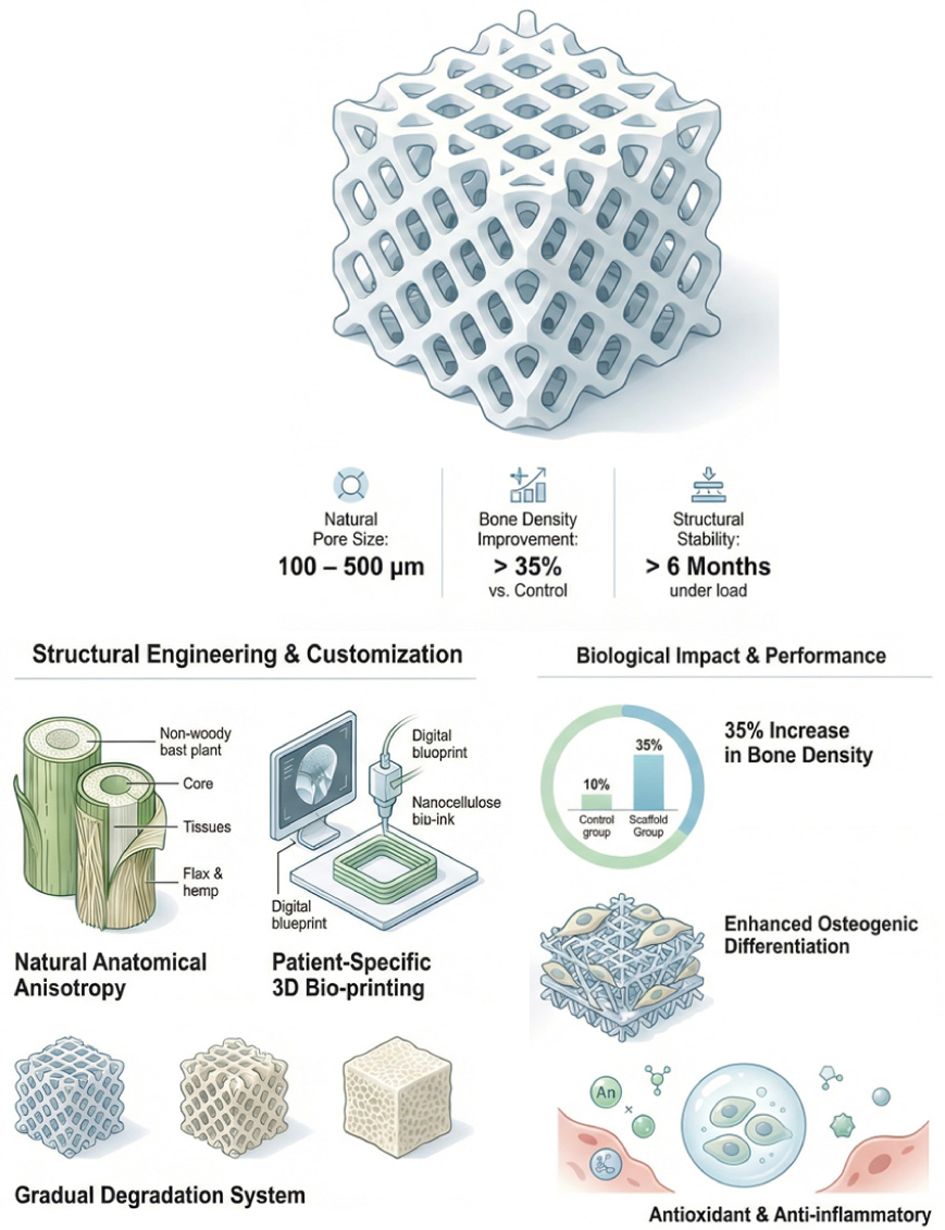
속대는 별도의 기공 형성 공정 없이도 100~500μm 크기의 상호 연결된 기공(Interconnected pores)을 가지고 있어, 블록 혹은 구형으로 가공하여 치조골(Alveolar bone) 혹은 두개골(Cranium) 부위의 충진재로 직접 활용한 사례가 있다[15,38]. 속대 표면에 하이드록시아파타이트(Hydroxyapatite, HAp)를 증착시킨 지지체는 골 결손 부위에 이식하였을 때, 천연 다공성 구조가 혈관 유입 통로 역할을 하여, 대조군 대비 골 밀도가 35% 이상 향상된 사례도 보고되었다[38, 39]. 속대 내 셀룰로오스 나노 섬유 표면에서 진행되는 무기질화 공정을 통해 실제 뼈와 유사한 무기질 성분을 생성하며, 자가 조직과의 생화학적 결착력을 극대화하여 조기 고정력을 만들어낼 수 있었다[39,40].
인피 섬유나 속대에서 추출한 나노 셀룰로오스를 바이오 잉크로 제작하여 3D 프린팅을 통해 정밀한 맞춤형 지지체 제작도 가능하다. 최근 연구에 따르면 인피 유래 나노 셀룰로오스 바이오 잉크를 이용하여 환자의 컴퓨터 단층촬영(Computed tomography) 데이터 기반 하악골(Mandible)과 대퇴골(Femur)의 복잡한 결손 형상을 정밀하게 모사한 맞춤형 지지체 관련 연구가 진행되었다[45,46]. 나노 셀룰로오스 바이오 잉크 내에 골수(Bone marrow) 유래 줄기세포(Stem Cell)를 담지하여 프린팅한 지지체는 일반 하이드로젤보다 알칼리성 인산가수분해효소(Phosphatase) 활성이 더 높게 관찰되었는데, 나노 단위의 결정 구조가 세포에 적절한 기계적 자극을 전달하여 골 분화를 촉진한 사례라 할 수 있다[41-44].
지지체의 항산화 및 항염증 성능 개선을 위해 리그닌 기반 복합소재 지지체도 개발되었다. 속대에서 추출한 리그닌 기반 나노섬유 지지체는 페놀계 작용기는 골 관절염(Arthritis) 부위의 과도한 활성 산소를 제거할 수 있다[2,51]. 또한, 리그닌-PLA 복합 지지체는 염증 환경 내에서 연골 세포의 사멸을 방지하고 연골 핵심 기질의 합성을 정상 수준으로 회복시킬 수 있어 생체 활성 소재로서 가능성도 확인하였다[2,39].
인피 섬유와 속대의 장점을 활용한 사례도 있다. 아마 나노 섬유를 외곽 프레임으로 사용하고 다공성 헴프 속대 분말을 내부 기지재로 혼용하여 인체의 계층적 골 구조를 정밀하게 모사함으로써, 하중 부하 조건에서도 구조적 변형 없이 6개월 이상의 장기 안정성을 유지하며, 실제 뼈의 재생 속도와 소재의 분해 속도를 동기화하는 단계적 분해(Gradual degradation) 시스템을 구현한 것이 좋은 사례이다[38,40,45].
4.2 정형외과용 고정 장치
비목질계 인피 자원을 활용한 정형외과용 고정 장치는 기존 금속 장치가 가지는 응력 차폐 현상을 해결하고, 환자의 생체 주기에 맞춰 스스로 분해되는 두 가지 특성을 모두 구현할 수 있다.
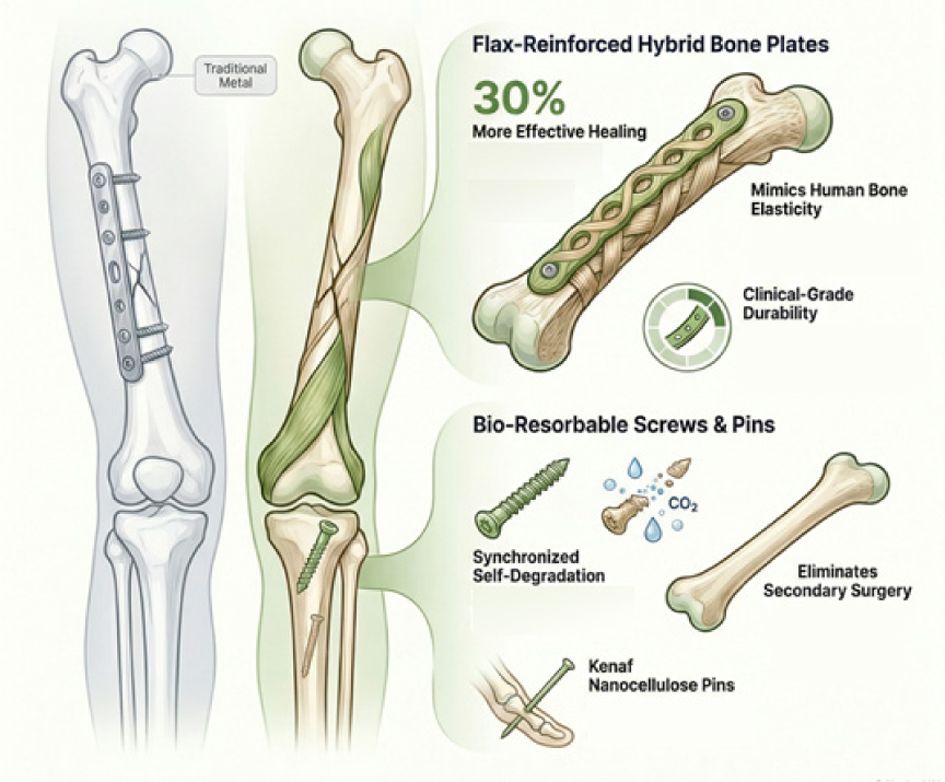
대표적인 사례가 아마 보강 하이브리드 골 고정판(Bone plate)이다. 피골질과 유사한 탄성 계수를 가지도록 설계된 아마 인피 섬유/탄소 섬유를 혼합 보강 에폭시 복합재 고정판은 골절 부위의 압축 하중을 금속 고정판보다 약 30% 더 효율적으로 뼈에 전달하여 자가 치우 기전을 활성화하였다[46]. 또한, 반복적인 보행 하중 환경을 모사한 피로 시험에서 106사이클 이상의 내구성을 확보하며, 실제 골절 유합(Malunion)이 완료되는 기간인 3~6개월 동안 구조적인 문제가 없음이 확인되었다[47,48]. 유사한 연구로는 아마와 저마 섬유를 각각 15%씩 혼합한 바이오 에폭시 복합재료의 인체 대퇴골 및 경골(Tibia)용 고정장치, 케블라와 아마 섬유를 혼합한 샌드위치 구조의 고정판 등이 있다[49,50].
4.3 치과용 골 이식재 및 재생막
비목질계 인피 자원은 치과 영역에서 치주 조직 유도재생술(Guided Tissue Regeneration) 및 골 유도 재생술(Guided Bone Regeneration)을 위한 고기능성 차단막과 골 이식재로 활용되고 있다. 특히 나노 셀룰로오스의 치밀한 구조와 속대의 천연 다공성은 연조직의 침투를 차단하고 치조골을 재생하는데 도움이 된다.
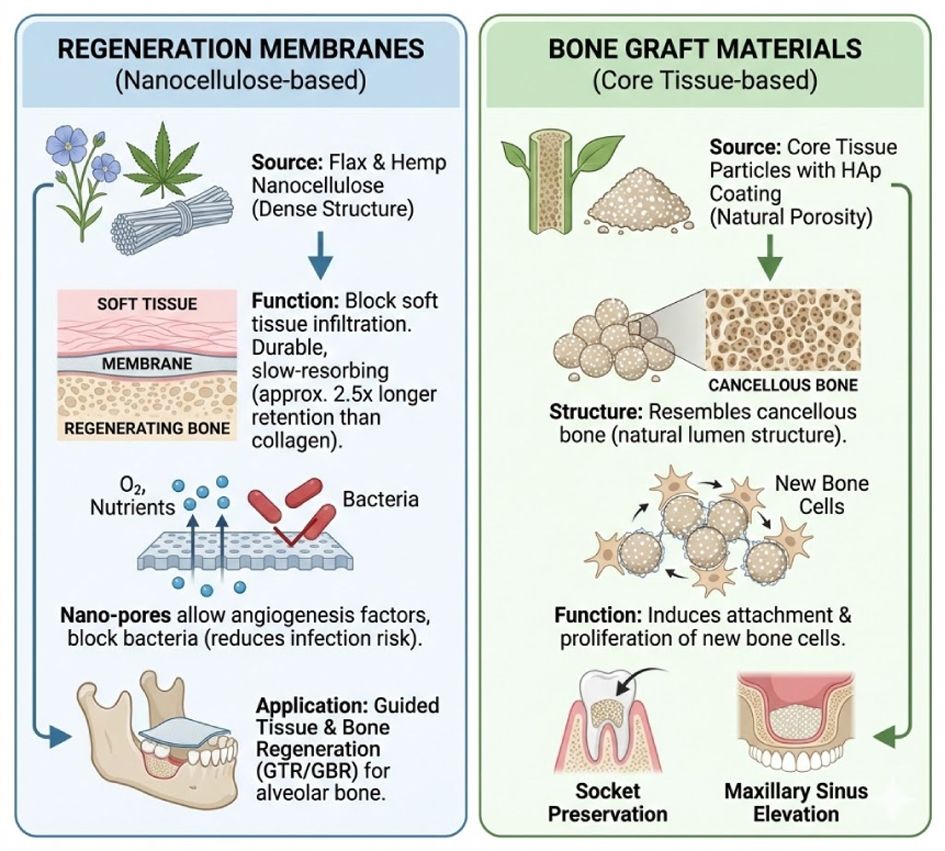
예를 들면 아마와 헴프 유래 나노 셀룰로오스를 활용하여 비흡수성/서방형(Sustained Release) 흡수 차단막을 제작한 사례를 들 수 있다. 나노 셀룰로오스 차단막은 젖은 상태에서도 높은 인장 강도를 유지하여, 기존 상용화된 콜라겐 막 대비 약 2.5배 긴 차단막 유지력을 보여 콜라겐 기반 막의 고질적 문제인 조기 붕괴를 해결하였다[51,52]. 또한, 나노 단위의 미세 기공 구조가 혈관 생성에 필요한 산소와 영향분은 통과시키고, 구강 내 세균의 침투는 물리적으로 차단하여 감염 위험도 낮추었다[53].
속대 조직의 천연 루멘 구조를 입자 형태로 가공하여 하이드록시아파타이트 코팅을 한 골 이식재는 해면골(Spongy Bone)과 유사하여, 신생 골 세포의 부착과 증식을 유도할 수 있어, 발치와 보존술 및 상악동 거상술(Sinus Lift)용 골 이식재로 활용되고 있다[54,55].
본 논문에서는 아마, 헴프, 양마와 같은 비목질계 인피 자원의 해부학적/화학적 특성을 분석하고, 이를 조직공학 및 재생공학, 정형외과 및 치과용 고정구와 같은 의료용 소재로 응용한 연구 및 실제 사례를 분석하였다.
2~3장에서는 원료의 구조적 특성과 생체 적합성을 다루었다. 인피 식물의 줄기는 고강도 인피 섬유와 다공성 속대로 구성되어, 하중 지지와 세포 내성을 동시에 만족시키는 다기능 구조 설계가 가능함을 알 수 있었다. 인피 식물의 핵심 성분인 셀룰로오소는 지지체의 기계적 형상 유지 역할을 담당하며, 리그닌은 항산화 및 항염증 기능을 통해 재생 미세환경을 만들어 준다. 인피 섬유와 속대는 물리적/화학적 개질을 통해 생체 내 분해 속도를 조절할 수 있어, 자가 조직의 치유 주기와 동기화하는 설계가 가능함을 확인하였다.
4장에서는 실제 의공학 응용 사례를 통해 비목질계 인피 자원의 활용성을 다루었다. 나노 셀룰로오스와 속대를 이용하여 조직 재생을 위한 지지체를 성공적으로 개발하였으며, 바이오 프린팅과 무기질화 공정을 통해 환자 맞춤형 골 및 연골 지지체를 구현할 수 있다. 아마와 헴프 등을 이용한 정형외과용 고정판 및 나사도 중요한 응용 사례인데, 금속 고정구와 달리 피질골과의 유사한 탄성 계수 구현을 통해 응력 차폐 문제를 성공적으로 해결하였다. 헴프 속대나 나노 셀룰로오스를 이용한 골 이식재나 차단막과 같은 치과용 응용도 보고되었다.
비목질계 자원은 생채 적합성과 기계적 정합성이라는 두 가지 장점으로 다양한 의공학적 응용이 가능하다는데 이견은 없을 것이다. 다만, 천연 원료라는 점에서 물성의 편차가 심하기 때문에 품질 표준화 및 불순물 제거 공정의 효율을 높이는 것이 중요하다. 또한, 생체 내 안정성과 분해 산물의 장기적 면역 반응에 대한 심층적인 분석도 필요하다. 향후 AI 기반의 복합재료 설계 기술과 친환경 추출 공정이 유기적으로 결합된다면, 금속 및 합성 고분자를 대체할 수 있는 지속 가능한 의공학적 소재가 될 것으로 전망된다. Fig. 1 Fig. 5

|
Fig. 1 Hierarchical representation of hemp stems; (a) cross-section model of hemp stem, (b) elementary hemp fiber structure, (c) lignocellulose structure |
|
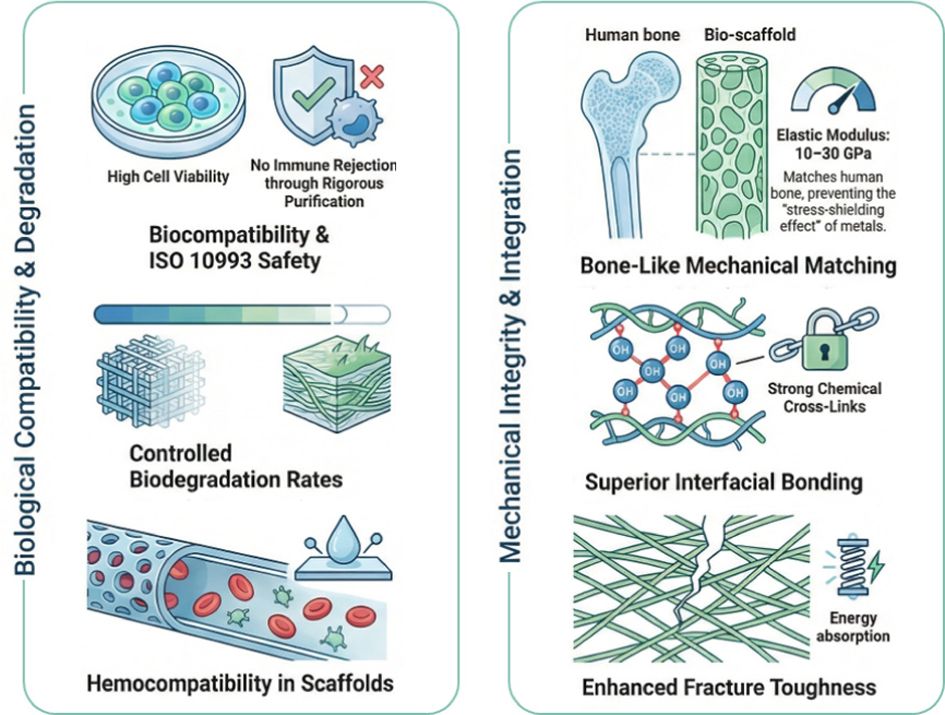
Fig. 2 Essential properties of non-woody resources for biomedical engineering |
|
Fig. 3 Schematic representation of engineering bone regeneration using non-woody resources |
|
Fig. 4 Schematic representation of bio-composite orthopedic fixation using non-woody resources |
|
Fig. 5 Schematic representation of dental bone graft materials and regeneration membranes using non-woody resources |
본 결과물은 2025년도 교육부 및 경상북도의 재원으로 경북RISE센터의 지원을 받아 수행된 지역혁신중심 대학지원체계(RISE)의 결과입니다. (B0080526002355)
- 1. Faruk, O., Bledzki, A.K., Fink, H., and Sain, M., “Biocomposites reinforced with natural fibers: 2000–2010,” Progress in Polymer Science, Vol. 37, No. 11, 2012, pp. 1552-1596.
-

- 2. Batra, S.K., Other Long Vegetable Fibers: Abaca, Banana, Sisal, Henequen, Flax, Ramie, Hemp, Sunn, and Coir, In Handbook of Fiber Chemistry (3rd ed.), CRC Press, Boca Raton, FL, 2007.
-

- 3. Ramesh, M., Hemp, jute, banana, kenaf, ramie, sisal fibers, In Testing and Characterization of Sustainable Bio-Composites, Woodhead Publishing, Cambridge, UK, 2018.
-

- 4. Eleutério, T., Trota, M.J., Meirelles, M.G., and Vasconcelos, H.C., “A Review of Natural Fibers: Classification, Composition, Extraction, Treatments, and Applications,” Fibers, Vol. 13, No. 9, 2025, 119.
-

- 5. Bourmaud, A., Morvan, C., Bouali, A., Placet, V., Perré, P., and Baley, C., “Relationships between Micro-Fibrillar Angle, Mechanical Properties and Biochemical Composition of Flax Fibers,” Industrial Crops and Products, Vol. 44, 2013, pp. 343-351.
-

- 6. Sorieul, M., Dickson, A., Hill, S., and Pearson, H., “Plant Fibre: Molecular Structure and Biomechanical Properties, of A Complex Living Material, Influencing Its Deconstruction Towards a Biobased Composite,” Materials, Vol. 9, No. 8, 2016, 618.
-

- 7. Vignesh, N.J., Rajesh Jesudoss Hynes, N., ShenbagaVelu, P., and Pravin, R., “A Survey on Characterization of Natural Fibers,” AIP Conference Proceedings, Vol. 2142, 2019, p. 150014.
-

- 8. Stochioiu, C., and Ciolcă, M., “Mechanical Characterization of Flax and Hemp Fibers Cultivated in Romania,” Materials, Vol. 17, No. 19, 2024, 4871.
-

- 9. Sayeed, M.M.A., Sayem, A.S.M., Haider, J., Akter, S., Habib, M.M., Rahman, H., and Shahinur, S., “Assessing Mechanical Properties of Jute, Kenaf, and Pineapple Leaf Fiber-Reinforced Polypropylene Composites: Experiment and Modelling,” Polymers, Vol. 15, No. 4, 2023, 830.
-

- 10. Scholz, M.S., Blanchfield, J.P., Bloom, L.D., Coburn, B.H., Elkington, M., Fuller, J.D., Gilbert, M.E., Muflahi, S.A., Pernice, M.F., Rae, S.I., Trevarthen, J.A., White, S.C., Bond, I.P., and Weaver, P.M., “The Use of Composite Materials in Modern Orthopaedic Medicine and Prosthetic Devices: A Review,” Composites Science and Technology, Vol. 71, No. 16, 2011, pp. 1791-1803.
-

- 11. Madhukiran, J., Rao, S.S., and Madhusudan, S., “Fabrication and Testing of Natural Fiber Reinforced Hybrid Composites Banana/Pineapple,” International Journal of Modern Engineering Research, Vol. 3, No. 4, 2013, pp. 2239-2240.
- 12. Ramanjaneyulu, C., Prasad, A.V.S.R., and Reddy, K.H.C., “Experimental Investigation of Mechanical, Thermal, DMA Analysis and Morphological Analysis on Abaca / Hemp / Kenaf,” Matéria (Rio de Janeiro), Vol. 29, No. 1, 2024, e20230234.
- 13. Stevulova, N., Cigasova, J., Estokova, A., Terpakova, E., Singovszka, E., and Holub, M., “Properties Characterization of Chemically Modified Hemp Hurds,” Materials, Vol. 7, No. 12, 2014, pp. 8131-8150.
-

- 14. Jawahar, P., Narmatha, M., and Vigneshkumar, M., “Mechanical Characterization of Kenaf Fiber (KF) and Jute Fiber (JF),” Journal on Materials and its Characterization, Vol. 3, No. 4, 2024, pp. 10-19.
-

- 15. Baghaei, B., Skrifvars, M., Rissanen, M., and Ramamoorthy, S.K., “Characterization of Hemp Fiber Reinforced PLA Composites,” Journal of Applied Polymer Science, Vol. 131, No. 15, 2014, 40534.
-

- 16. George, J., and Sabapathi, S.N., “Cellulose Nanocrystals: Synthesis, Functional Properties, and Applications,” Nanotechnology, Science and Applications, Vol. 8, 2015, pp. 45-54.
-

- 17. Aziz, T., Fan, H., Khan, F.U., Haroon, M., and Cheng, L., “A Review on the Modification of Cellulose and Its Applications,” Polymers, Vol. 14, No. 15, 2022, 3206.
-

- 18. Di, J., Li, J., Sun, C., Xu, L., and Li, X., “Advances in Cellulose-Based Hydrogels for Drug Delivery: Preparation, Modification and Challenges,” Gels, Vol. 11, No. 12, 2025, 938.
-

- 19. del Olmo, J. A., Martínez, V. S., de Cestafe, N. M., Alonso, J. M., Olavarrieta, C., de Heredia, M. U. L., Sandra Benito Cid, and González, R. P., “Effectiveness Evaluation of Hyaluronic Acid-Based Commercial Eye Drops to Treat Ophthalmic Dry Eye Disease,” Carbohydrate Polymer Technologies and Applications, Vol. 8, 2024, p. 100577.
-

- 20. Chen, M., Li, Y., Liu, H., Zhang, D., and Shi, Q.S., “High Value Valorization of Lignin as Environmental Benign Antimicrobial,” Materials Today Bio, Vol. 18, 2022, 100520.
-

- 21. Yang, W., Owczarek, J.S., Fortunati, E., Kozanecki, M., Mazzaglia, A., Balestra, G.M., Kenny, J.M., Torre, L., and Puglia, D., “Antioxidant and Antibacterial Lignin Nanoparticles in Polyvinyl Alcohol/Chitosan Films for Active Packaging,” Industrial Crops and Products, Vol. 94, 2016, pp. 800-811.
-

- 22. United States Pharmacopeia, USP chapter <161>, Transfusion and Infusion Assemblies and Similar Medical Devices, USP Convention, Rockville, MD.
- 23. Figueiredo, P., Lintinen, K., Kiriazis, A., Hynninen, V., Liu, Z., Bauleth-Ramos, T., Rahikkala, A., Correia, A., Kohout, T., Sarmento, B., Yliperttula, M., Kostiainen, M.A., and Santos, H.A., “In vitro Evaluation of Biodegradable Lignin-based Nanoparticles for Drug Delivery and Enhanced Antiproliferation Effect in Cancer Cells,” Biomaterials, Vol. 121, 2017, pp. 97-108.
-

- 24. Han, F., Wang, J., Ding, L., Hu, Y., Li, W., Yuan, Z., Guo, Q., Zhu, C., Yu, L., Wang, H., and Zhao, Z., “Tissue Engineering Scaffolds,” Frontiers in Bioengineering and Biotechnology, Vol. 8, 2020, 83.
- 25. Leal, B.B.J., Wakabayashi, N., Oyama, K., Kamiya, K., Braghirolli, D.I., and Pranke, P., “Vascular Tissue Engineering: Polymers and Methodologies for Small Caliber Vascular Grafts,” Frontiers in Bioengineering and Biotechnology, Vol. 8, 2021, 583217.
-

- 26. International Organization for Standardization, Biological Evaluation of Medical Devices—Part 5: Tests for In Vitro Cytotoxicity (ISO Standard No. 10993-5:2009), ISO, Geneva, Switzerland, 2009.
-

- 27. Namvar, F., Jawaid, M., Tahir, P.M., Mohamad, R., Azizi, S., Khodavandi, A., Rahman, H.S., and Nayeri, M.D., “Potential Use of Plant Fibres and Their Composites for Biomedical Applications,” BioResources, Vol. 9, No. 3, 2014, pp. 5688-5706.
-

- 28. Endes, C., Camarero-Espinosa, S., Mueller, S., Foster, E.J., Petri-Fink, A., Rothen-Rutishauser, B., Weder, C., and Clift, M.J.D., “A Critical Review of The Current Knowledge Regarding The Biological Impact of Nanocellulose,” Journal of Nanobiotechnology, Vol. 14, 2016, 78.
-

- 29. Pereira, M.M., Raposo, N.R.B., Brayner, R., Teixeira, E.M., Oliveira, V., Quintão, C.C.R., Camargo, L.S.A., Mattoso, L.H.C., and Brandão, H.M., “Cytotoxicity and Expression of Genes Involved in The Cellular Stress Response and Apoptosis in Mammalian Fibroblast Exposed to Cotton Cellulose Nanofibers,” Nanotechnology, Vol. 24, No. 7, 2013, 075103.
-

- 30. Basu, A., Hong, J., and Ferraz, N., “Hemocompatibility of Ca2+-crosslinked Nanocellulose Hydrogels: Toward Efficient Management of Hemostasis,” Macromolecular Bioscience, Vol. 17, No. 11, 2017, 1700236.
-

- 31. Pei, B., Wang, W., Fan, Y., Wang, X., Watari, F., and Li, X., “Fiber-Reinforced Scaffolds in Soft Tissue Engineering,” Regenerative Biomaterials, Vol. 4, No. 5, 2017, pp. 257-268.
-

- 32. Khouaja, A., Koubaa, A., and Daly, H.B.., “Mechanical and morphological properties of cellulose biocomposites,” Chemosphere, Vol. 379, 2025, 144415.
-

- 33. Bhatnagar, P., Law, J.X., and Ng, S.F., “Evaluation of a Kenaf Nanocrystalline Cellulose-based Hydrogel Containing Platelet Lysate for Full-thickness Wound Healing,” Recent Advances in Drug Delivery and Formulation, Vol. 19, No. 1, 2025, pp. 72-85.
-

- 34. Bagheri, Z.S., Tavakkoli Avval, P., Bougherara, H., Aziz, M.S.R., Schemitsch, E.H., and Zdero, R., “Biomechanical Analysis of a New Carbon Fiber/Flax/Epoxy Bone Fracture Plate Shows Less Stress Shielding Compared to a Standard Clinical Metal Plate,” Journal of Biomechanical Engineering, Vol. 136, No. 9, 2014, 091002.
-

- 35. Al-Tamimi, A.A., Quental, C., Folgado, J., Peach, C., and Bartolo, P., “Stress analysis in a bone fracture fixed with topology-optimised plates,” Biomechanics and Modeling in Mechanobiology, Vol. 19, No. 2, 2019, pp. 693-699.
-

- 36. Senthil Maharaj, P.S.R., and Vasanthanathan, A., “An Insight into The Mechanical and Tribological Behavior of Carbon-Flax Reinforced Bioepoxy Hybrid Composite Bone Plates for Orthopedic Applications,” Polymers and Polymer Composites, Vol. 31, 2023, pp. 1-12.
-

- 37. Fadhil, H.X., Hamad, Q.A., Oleiwi, J.K., and Ibrahim, N.F., “Investigations of Flexural and Impact Properties of Bio-Epoxy-Based Composites for Bone Plate Application,” Engineering and Technology Journal, Vol. 43, No. 12, 2025, pp. 1084-1095.
-

- 38. J Khan, M.U.A., Razak, S.I.A., Ansari, M.N.M., Zulkifli, R.M., Ahmad Zawawi, N., Arshad, M., “Development of Biodegradable Bio-Based Composite for Bone Tissue Engineering: Synthesis, Characterization and In Vitro Biocompatible Evaluation,” Polymers, Vol. 13, 2021, 3611.
-

- 39. Liu, X., Wang, B., Ma, J., and Hu, H., “3D-Printed Heterogeneous Biomimetic Scaffold Utilizing TEMPO-Oxidized and Mineralized Bacterial Cellulose Nanofibers for Osteochondral Regeneration,” Carbohydrate Polymers, Vol. 370, 2025, 124366.
-

- 40. Akter, M., Uddin, M.H., and Tania, I.S., “Biocomposites based on natural fibers and polymers: A review on properties and potential applications,” Journal of Reinforced Plastics and Composites, Vol. 41, No. 17-18, 2022, pp. 705-742.
-

- 41. Sultan, S, and Mathew, A.P., Three-dimensional Printing of Nanocellulose-Based Hydrogels, In: Jose, J., Thomas, S., Thakur, V.K. (eds) Nano Hydrogels. Gels Horizons: From Science to Smart Materials. Springer, Singapore, 2021.
-

- 42. Sharma, C., Raza, M.A., Purohit, S.D., Pathak, P., Gautam, S, Corridon, P.R., and Han S.S., “Cellulose-based 3D Printing Bio-inks for Biomedical Applications: A Review,” International Journal of Biological Molecules, Vol. 305, No. 2, 2025, 141174.
-

- 43. Sreedharan, M., Vijayamma, R., iyaskina, E., Revin, V.V., Ullah, M.W., Shi, Z., Yang, G., Grohens, Y., Kalarikkal, N., Khan, K.A., and Thomas, S., “Nanocellulose-Based Scaffolds for Skin and Bone Tissue Engineering: A 10-Year Overview,” Biomacromolecules, Vol. 25, No. 4, 2024, pp. 2136-2155.
-

- 44. Liang, R., Yang, X., Yew, P. Y. M., Sugiarto, S., Zhu, Q., Zhao, J., Loh, X. J., Zheng, L., and Kai, D., “PLA-Lignin Nanofibers as Antioxidant Biomaterials for Cartilage Regeneration and Osteoarthritis Treatment,” Journal of Nanobiotechnology, Vol. 20, 2022, 327.
-

- 45. Hwazen, S.F., Qahtan, A.H., and Jawad, K.O., “Fabrication and biological evaluation of bio-epoxy hybrid composites reinforced with flax, glass, carbon, and polyethylene fibers for bone plate applications,” Annales De Chimie. Science Des Materiaux, Vol. 49, No. 2, 2025, pp. 187-193.
-

- 46. Kennedy, S.M., Aruachalam, V., and Kannan, A., “A Novel Carbon-Flax Bioepoxy Hybrid Composite Bone Plate with Enhanced Bio-Mechanical Performance,” Materials Science and Engineering Technology, Vol. 55, No. 4, 2024, pp. 508-517.
-

- 47. Kumar, S.S., Aravindh, M., Manoj, V.K., Madhumithra, C., Kaviya, P., and Yaswanth, S., “Fracture toughness of bio-fiber reinforced polymer composites- a review,” Materials Today: Proceedings, In Press, 2023.
-

- 48. Kumar, S., Zindani, D., and Bhowmik, S., “Investigation of Mechanical and Viscoelastic Properties of Flax- and Ramie-Reinforced Green Composites for Orthopedic Implants,” Journal of Materials Engineering and Performance, Vol. 29, 2020, pp. 3161-3171.
-

- 49. Gashawtena, E., Sirahbizu, B., and Kidane, A., “Review on Alternate Materials for Producing Low Cost Lower Limb Prosthetic Socket,” Journal of Material Sciences & Engineering, Vol. 10, No. 6, 2021, pp. 1-6.
- 50. Fadhil, H.S., Oleiwi, J.K., and Hamad, Q.A., “Investigation of Tensile, and Morphological Characteristic of Laminated Bio-Composite for Bone Plate Fixation Applications,” Journal of Composite and Advanced Materials, Vol. 35, No. 2, 2025, pp. 295-302.
-

- 51. Kuscu, S., Baysan, F.D., Korkmaz, N., Kuscu, A.I., and Karadag, A., “Enhancing Mechanical Properties Of Glass-Ionomer Cement with Hemp Fiber: A Sustainable Approach for Dental Restorations,” BMC Oral Health, Vol. 25, 2025, 369.
-

- 52. Baysan, F.D., Kuscu, S., Korkmaz, N., and Celebi, N., “Evaluation of the Effects of Hemp Fiber Addition on Fracture Strength, Acrylic Tooth Bonding and Water Absorption of Polymethyl Methacrylate,” Selcuk Dental Journal, Vol. 12, No. 1, 2025, pp. 14-19.
-

- 53. Kuscu, S., Baysan, F.D., and Korkmaz, N., “Effect of Addition of Hemp Fiber and Lignin-pectin-free Hemp Fiber to Poly(methyl methacrylate) on Surface Roughness Property,” BMC Oral Health, Vol. 25, 2025, 847.
-

- 54. Sheng, S.B., Alawi, R., Johari, Y., Muttlib, N.A.A., Hussin, M.H., Mohamad, D/, and Karobari, M.I., “Effects of Fiber Loading on Mechanical Properties of Kenaf Nanocellulose Reinforced Nanohybrid Dental Composite Made of Rice Husk Silica,” Journal of Functional Biomaterials, Vol. 14, No. 4, 184.
-

- 55. Abbas, H., Characterization of Fiber Reinforced Nanohybrid Dental Composites from Agricultural Biowaste Using Kenaf Fiber. Masters thesis, Universiti Sains Malaysia, 2022.
 This Article
This Article
-
2026; 39(1): 34-42
Published on Feb 28, 2026
- 10.7234/composres.2026.39.1.034
- Received on Feb 5, 2026
- Revised on Feb 8, 2026
- Accepted on Feb 11, 2026
 Services
Services
- Abstract
1. 서 론
2. 비목질계 자원의 분류 및 특성
3. 의공학적 응용을 위한 비목질계 자원의 요구 특성
4. 의공학적 응용
5. 결 론
- 후기
- References
- Full Text PDF
Shared
 Correspondence to
Correspondence to
- Hui-Yun Hwang
-
School of Electronics and Mechanical Engineering, Gyeongkuk National University
- E-mail: hyhwang@gknu.ac.kr






 Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.
Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.