- 리튬이온전지 양극용 프러시안블루계 소재 동향
Hyunjoon Yoo*, Sang Bok Lee**, Il-Kwon Oh*†
* National Creative Research Initiative for Functionally Antagonistic Nano-Engineering, Department of Mechanical Engineering, Korea Advanced Institute of Science and Technology (KAIST), Yuseong-gu, Daejeon, Republic of Korea
** Department of Chemistry and Biochemistry, Maryland NanoCenter, Institute for Research in Electronics and Applied Physics, Department of Materials Science and Engineering, University of Maryland, College Park, MD 20742, USA- Prussian Blue Cathodes for Lithium-Ion Batteries: A Review
유현준* · 이상복** · 오일권*†
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Prussian blue (PB) and Prussian blue analogues (PBAs) are being revisited as low-cost cathode candidates for lithium-ion batteries (LIBs), owing to their three-dimensional open-framework structures that facilitate favorable ion-diffusion pathways and their compositional tunability using relatively abundant elements such as Fe and Mn. In aqueous electrolytes, their kinetics and power capability can be relatively favorable due to fast ion transport and reduced desolvation barriers, whereas in non-aqueous electrolytes water content and defects, low electronic conductivity, and interfacial reactions often increase polarization and accelerate degradation. This review summarizes Li storage behavior and voltage characteristics of PB based cathodes and compares practical strategies such as defect and water control, compositing, and CEI design. We also discuss remaining challenges from electrolyte selection and electrode engineering perspectives to achieve both high power and stable cycling.
프러시안블루(Prussian blue, PB) 및 프러시안블루 유사체(PBA)는 3차원 개방형 골격 구조를 기반으로 이온 확산 경로가 유리하고, Fe/Mn 등 비교적 풍부한 원소 조합으로 설계가 가능해 저가형 리튬이온전지 양극 후보로 다시 논의되고 있다. 수계 전해질에서는 빠른 이온 이동과 낮은 탈용매화 장벽으로 비교적 고출력/가역 구동이 용이하지만, 유기 전해질에서는 수분과 결함, 낮은 전자전도도, 계면 반응으로 인해 분극과 열화가 커지는 한계가 있다. 본 리뷰는 PB계 양극의 리튬 저장 반응과 전압 특성을 정리하고, 결함과 수분 제어, 복합화, CEI 설계가 성능에 미치는 영향을 비교한다. 또한 출력과 안정성을 함께 확보하기 위해 필요한 전해질 선택과 전극 설계 관점의 과제를 논의한다.
Keywords: 프러시안블루(Prussian blue), 프러시안블루 유사체(Prussian blue analogue), 리튬이온배터리(Lithium-ion battery), 양극(Cathode), 양극 전해질 계면(Cathode electrolyte interphase)
리튬이온전지(LIB)의 양극은 안전성, 수명, 원가, 및 자원 리스크를 동시에 만족해야 하며, 이러한 요구는 전기차의 보급 확대와 대규모 ESS 적용이 늘어나면서 더욱 강화되고 있다[1–4]. 상용 양극재로 많이 활용되는 LFP(LiFePO4)는 안전성과 장수명 측면에서 강점이 있으나, 상대적으로 낮은 작동전압 및 에너지 밀도, 그리고 저온 및 고율 조건에서의 출력 저하가 반복적으로 지적되어 왔다[2,3,5,6]. 이런 배경에서 Prussian blue (PB)/Prussian blue analogues(PBA)는 철, 망간 등 비교적 풍부한 원소 기반 조성으로 설계가 가능하고, AxM’[M(CN)₆]1-γ□γ·nH2O 형태의 개방형 골격(open framework)을 통해 이온 저장을 구현할 수 있어 저원가 양극 후보로 논의되어 왔다[7–9]. PB/PBA는 이미 수계 전해질에서 Na+/K+/Zn2+/Mg2+ 등 다양한 이온 저장이 보고되어 왔으며[10–12], 3차원 채널 기반의 삽입/탈리 특성이 잠재적으로 빠른 반응성을 제공할 수 있다.
그러나 비수계 유기 전해질 기반 LIB 양극으로의 본격적 확장에는 여전히 뚜렷한 난제가 있다. 첫째, 수용액 공침 기반 PB/PBA는 [M(CN)6] 공공(Vacancy)과 수분(zeolitic/interstitial, coordinated water), 표면-OH를 동반하기 쉬우며, 이들이 비수계에서는 초기 CEI 형성과 전극 반응 경로를 바꿔 가역 용량·수명에 직접 영향을 준다[5,8,11,12]. 둘째, 다수의 폴리아니온계 골격(e.g. FePO4, VOPO4)에서 관찰되는 Li 삽입 전위가 Na 대비 높다는 이점이 Li-PBA 계열에서는 제한적이며, 더 근본적으로는 큰 공극을 갖는 PBA 골격과 작은 Li+ 사이의 결정화학적 부정합이 제기된다. 실제로 Na+를 Li+로 치환할 경우 PBA 구조의 분해/재배열이 유도될 수 있는데, Xiao 등은 MnFe(CN)6에서 Li+의 더 짧은 Pauli 반발 반경 때문에 Li+가 Na+보다 N에 더 가깝게 위치하려는 경향을 보이며, 그 결과 MnN6 옥타헤드라가 LiN4 및 MnN4 사면체로 진화하는 구조 변화를 보고하였다[13, 14]. 셋째, PB/PBA 자체의 낮은 전자전도도(대략 10-11-10-7 S·cm-1)와 비교적 큰 밴드갭(대략 1.9-4.9 eV)은 고율에서 분극을 키워 출력 관점에서 불리하게 작용한다[15,16]. 넷째, Mn 등 Jahn-Teller 활성 금속을 포함한 일부 조성에서는 충/방전 중 구조 왜곡 및 전이금속 용출이 촉진되어 장수명 안정성이 약화될 수 있다[12,17–19].
최근에는 이러한 한계를 보완하기 위해 저결함/저수화 프레임워크 합성 및 결함 치유를 통한 초기 상태 정밀 제어[20], 리치에이션(Pre-lithiation)을 통한 Li-rich 초기 상태 설계로 비수계에서의 가역성/안정성 개선[13,21], CEI(Cathode-Electrolyte Interface) 엔지니어링을 통한 계면 반응 제어[22]와 높은 전도성을 지니는 물질과의 복합화[23]등이 제시되고 있다.
기존의 PB/PBA 리뷰들은 PB계 전극의 결정화학, 결함/수화도, 이온 저장 메커니즘을 폭넓게 정리해 왔으나, 주된 초점은 Na+/K+ 등 비리튬 시스템의 양극 응용에 맞춰져 있고, 비수계 LIB에서의 PB/PBA 양극 적용은 제한된 분량으로 다뤄지거나 소재의 장/단점이 서로 분절된 형태로 제시되는 경우가 많다[24–26]. 이에 본 리뷰는 비수계 리튬이온전지용 PB/PBA 양극을 세 가지 상호연결된 설계 관점에서 재조명하고자 한다. 첫째, [M(CN)6] 공공과 잔존 수분이 활성 레독스 사이트의 접근성, 계면 반응성, 그리고 초기 비가역 거동에 미치는 영향을 살펴본다. 둘째, 본질적으로 Li-free 출발 조성을 갖는 PB/PBA 프레임워크에서 가역적인 리튬 저장을 구현하기 위해 필요한 초기 lithiation 상태와 prelithiation 전략의 중요성을 논의한다. 셋째, 전도성 복합화와 CEI 제어를 포함한 전극 및 계면 수준의 설계 전략이 고율 특성과 사이클 안정성 향상에 어떻게 기여하는지를 정리한다. 즉, 본 논문은 PB/PBA 화학 전반을 폭넓게 나열하기보다는, 비수계 LIB 구동에서결정적으로 작용하는 요인에 초점을 두며, Na 이온전지 관련 연구는 필요한 경우 기작의 이해를 돕기 위한 보조적 맥락으로만 활용한다.
PB/PBA는 일반적으로 면심입방(fcc) 기반 골격에서 금속–시안화물–금속의 선형 결합(–C≡N–)으로 연결된 3차원 네트워크를 형성한다[7–9]. 개방형 골격(AxM’[M(CN)₆]1-γ □γ·nH2O)의 A-site에는 알칼리 금속이 채널/공간을 점유할 수 있으며, M’–M 레독스 조합이 전자구조와 반응전압을 결정하고, 동시에 삽입 과정에서의 국소 배위 변화 및 격자 변형에 영향을 준다[27,28]. 특히 PB/PBA의 개방형 채널은 비교적 큰 Na+/K+의 삽입·탈리를 허용하고, 프레임워크는 반복적인 삽입 과정에서 부피 변화에 대해 일정 수준의 구조적 완충 능력을 보이는 것으로 알려져 있다. 이러한 특징은 Na/K 시스템에서 3 V 내외의 실용 전압과 우수한 고율 특성으로 보고되어 왔으며[7,10,11], 같은 골격 관점에서 Li+에 대해서도 삽입 반응 자체는 초기부터 가능하다고 제시되었다[29,30].
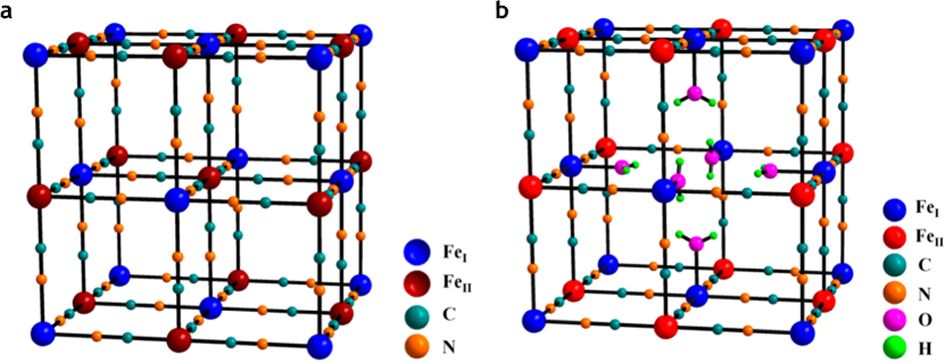
실제 합성된 PB/PBA는 이상적인 완전 골격과 달리, 수용액 공침 과정에서 [M(CN)6]이 결손되는 공공(□)이 형성되기 쉽고, 이에 수분이 잔존하는 경우가 많다(Fig. 1)[5,8,11,12]. 이들은 단순한 불순물이 아니라 유효 레독스 사이트 수, 공공 주변의 국소 전하/조성 분포, 금속–CN 배위환경을 바꾸어 리튬 삽입 반응의 자리와 경로를 달라지게 하는 구조적 변수로 작동한다. 따라서 PB/PBA의 반응성을 논할 때는 공공/수화의 여부가 아닌, 공공의 농도와 분포, 물의 형태(zeolitic/interstitial vs coordinated), 그리고 그에 따른 국소 배위 변화를 함께 규정하는 접근이 필요하다.
특히 비수계 LIB에서 PB/PBA에 잔존한 수분(또는 -OH)은 충/방전 초기 탄산염 전해질과 반응하여 CEI의 조성과 성장 속도를 바꾸며, 그 결과 초기 사이클에서 쿨롬 효율 저하, 전압 프로파일/분극 변화를 보인다[22,30,31]. 또한 수분과 공공은 금속 주변의 배위환경을 바꾸어 금속의 산화수 분포 및 전자상태를 변화시키므로, 동일 조성이라도 합성 품질(공공/수화도)에 따라 반응 전압과 가역성이 달라질 수 있다. Asakura 등은 XAFS 기반 국소구조 분석을 통해 PBAs에서 결함과 수화가 금속–리간드 배위환경을 어떻게 변화시키는지 제시함으로써, 공공/수화가 단순 불순물이 아니라 결정화학적 설계변수임을 보여주었다[31].
비수계 LIB 관점에서 수분 제거는 단순히 건조 여부가 아니라, 어떤 형태의 물(zeolitic/interstitial, coordinated)을 어디까지 제거할지(구조 안정성 유지)까지 포함하는 문제이다. 예를 들어, LiFeHCF의 경우 결정 격자에 zeolitic 물이 존재하면 온도가 증가함에 따라 탈수에 의한 구조변화가 시작되며, 비대칭 Fe-C6/Fe-N6 팔면체 증가에 의해 결정 구조의 부정적인 영향을 미친다[13]. 비슷한 현상이 PB/PBA의 소듐 전지 연구에서도 관측되며, in situ heating-XRD 기반 연구에서 PBA가 150°C 이하에서는 구조 변화가 거의 없고, 150–200°C 이상에서 조성/결함도에 따라 상전이가 시작되며, 250°C 이상에서는 특정 조성에서 구조 붕괴/열분해가 유발될 수 있음을 보고하였다[32]. 또한, PBA/Prussian white의 탈수는 온도, 가열속도와 분위기(진공/불활성) 및 분말과 복합전극(바인더/탄소 포함) 환경에 의해 동역학적으로 달라질 수 있어, 최적 건조 조건이 분말과 전극에서 다를 수 있다[33].
따라서 실용적으로는 진공 또는 불활성 분위기에서의 단계적 건조(zeolitic/interstitial, coordinated의 선택적 제거), 무수 용매 세정/치환 후 진공 건조를 통한 표면 수분 저감, 건조 후 셀 공정을 저습 환경에서 진행하여 재흡습을 억제, 탄소/전도성 고분자 코팅을 통해 재흡습과 계면 부반응을 동시에 억제하는 접근이 유효하다.
일반적으로 파우더 형태의 NCM 등은 약 120°C 진공 오븐에서 처리 후 재흡습과 carbonate 불순물 생성을 방지하기 위해 저습 환경에서 보관한다. 복합전극의 경우에서도, 슬러리 캐스팅 이후 binder migration 방지를 위해 60-120°C hot dryer에서 건조 이후, 120-150°C 환경(진공 오븐 혹은 roll-to-roll용 hot air)에서 용매를 제거한다. 다만 PB/PBA의 경우 수분 제거에 따른 구조변화가 배터리의 성능 열화에 미치는 영향은 아직까지 체계적으로 분석되지 않았고, 고온 열처리를 통해 합성되는 기존 활물질과 달라 열적 안정성에 대한 추가적인 평가가 이루어 져야한다. 이에, 사용 환경에 따라 공정 별 TGA/FT-IR(수분 잔존), XRD(상변화), 그리고 전기화학 임피던스(계면 저항)로 함께 검증하는 것이 바람직하다.
전자구조 측면에서 PB계는 낮은 고유 전도도와 상대적으로 큰 밴드갭으로 인해 고율에서 전하이동 저항이 커질 수 있으며, 이는 출력 저하뿐 아니라 과전압 증가에 따른 발열/열화 가속과도 연결된다. DFT 기반 전자구조 분석과 수송 모델링에 따르면, PB/Prussian white/Berlin green 계열은 조성 및 결함 상태에 따라 밴드구조와 캐리어 수송성이 크게 달라지고, 동일한 구조라도 공공과 수화가 전자구조를 유의미하게 변형시킨다[15,16]. 따라서 LIB 양극 설계에서는 공공/수화도를 단순히 줄이는 것이 아니라, 어떤 공공이 어느 정도 존재할 때 Li+ 확산/계면 안정/전자수송이 동시에 최적화되는지를 규명해야 한다.
|
Fig. 1 Schematic illustration of the crystal structure of Fe-based Prussian blue. (a) Defect-free Prussian blue framework and (b) framework containing vacancies and hydration. Reprinted with permission from [20] |
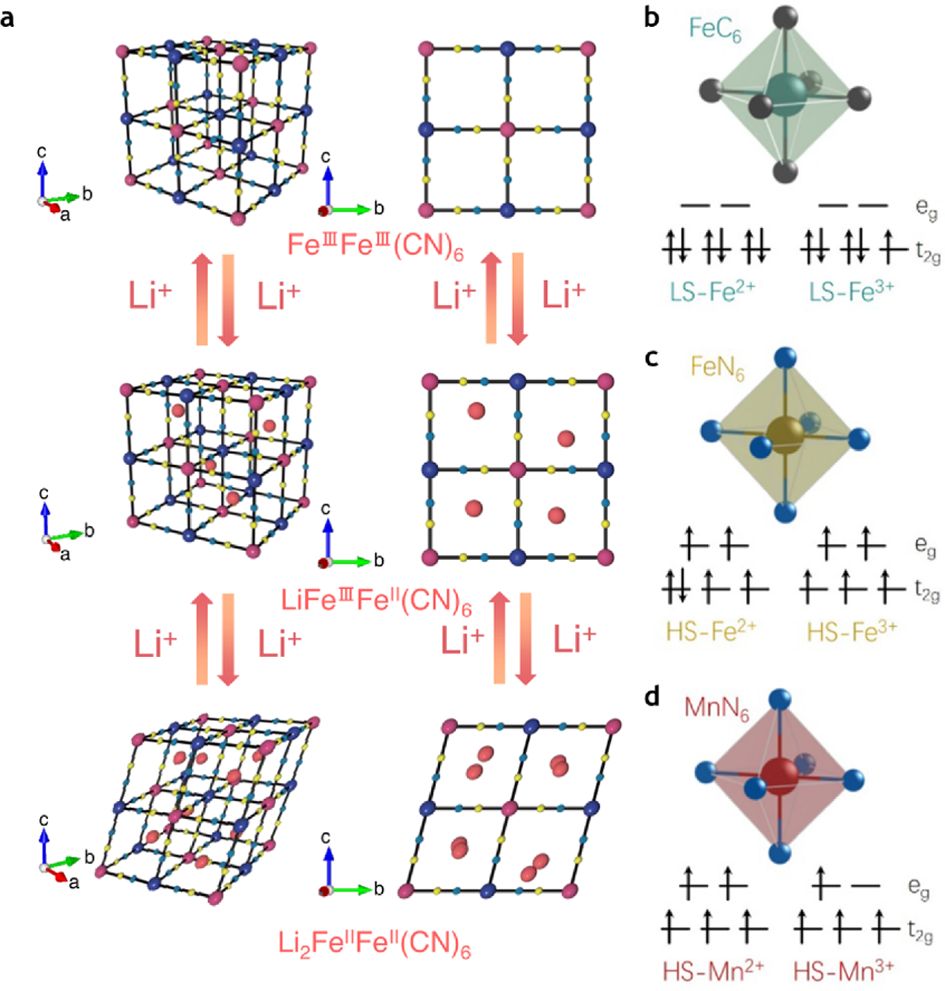
PB계는 리튬 이온 배터리에서, Fe 기반 레독스 커플을 통해 2-electron 반응(Li2FeIIFeII(CN)6 - LiFeIIFeIII(CN)6 - FeIIIFeIII(CN)6)이 가능하며, 이러한 다전자 반응 가능성은 약 175 mAh g-1[21]에서 최대 190 mAh g-1[13] 수준의 이론용량을 지닌다(Fig. 2a). 이는 기존 상용 양극재인 LFP의 비용량(~170 mAh g-1)과 비교하여도 높은 수준이다.
PB/PBA에서의 전기화학 반응은 금속 레독스(M’/M)와 삽입 이온(A-site)의 상호작용으로 기술되며, 전하보상은 금속의 산화수 변화와 삽입 이온의 농도 변화가 결합된 형태로 나타난다[8,27,28]. 특히 CN- 리간드 장에서 형성되는 결정장 분할에 따라 Fe 및 Mn 중심의 저스핀(LS)/고스핀(HS) 상태와 t2g/e_g 점유가 달라지며, 이는 레독스 전위와 구조 안정성의 차이로 이어진다(Fig. 2b-d). 예를 들어 Fe–C₆/Fe–N₆ 팔면체에서 LS-Fe2+/Fe3+는 e_g 점유가 억제되어 국소 왜곡 구동력이 상대적으로 작고, 반면 HS-Mn3+는 e_g 전자 점유로 인해 Jahn–Teller 활성이 커져 충/방전 반복 시 팔면체 왜곡 및 상전이 가능성을 높인다[34]. 실제 전지에서는 이러한 벌크 전자구조 효과가 계면(CEI)과 결함/수분의 영향과 함께 나타나 전위와 가역성을 좌우한다. 그럼에도 전자구조-격자 결합 특성은 Na/K 시스템에서 비교적 높은 실용 전압(대개 3 V 내외)과 준수한 속도를 보이는 경향을 설명한다. 반면 Li 시스템에서는 더 강한 용매화/탈용매화 장벽, 비수계에서의 CEI 형성, 수분/결함과 결합된 복잡한 전하보상 메커니즘이 겹치며 kinetics가 느려지기 쉽다는 점과도 맞물린다[19,29]. 따라서 Li-PB/PBA에서는 조성(Fe/Mn) 선택뿐 아니라, 스핀 상태, 국소 배위 변화, 결함/수분, 계면을 함께 고려한 설계가 필요하다.
초기 연구로 Imanishi 등은 철 시안화물 복합체의 Li 삽입 거동을 양극 관점에서 보고하여, PB계 프레임워크가 Li 저장을 수행할 수 있음을 실험적으로 제시하였다[30]. 이후 Shen 등은 PB(또는 iron cyanide)의 개방 프레임워크가 Li 이온의 수송 및 저장에 공간적 여유(room)를 제공한다는 관점에서 PB를 LIB 양극 후보로 정리하였고, Fe4[Fe(CN)6]3 및 FeFe(CN)6에서 각각 약 95 mAh g-1 및 138 mAh g-1의 가역 용량을 보고하였다[29]. 이 결과는 PB계의 양극 가능성을 보여주었으나, 동시에 결함/수화/계면 안정성이 성능을 지배한다는 문제의식을 명확히 했다.
최근의 진전은 초기 상태 설계에 있다. Wu 등은 공침 합성에서 흔한[Fe(CN)6] 공공과 구조수가 Li+ 삽입의 가역성을 해친다는 점에 착안해, 초기부터 저결함(near defect-free) FeFe(CN)6 골격을 목표로 설계했다. 이를 위해 K3Fe(CN)6를 단일 철 소스로 한 산성 조건의 hydrolytic precipitation을 적용해 단결정 나노큐브 형태로 결함/수분을 최소화했고, 그 결과 결함 제어가 LIB 성능에 직접 연결됨을 보여주었다[20]. 더 나아가 Zhang 등은 lithiated PBA를 비수계 LIB에서 안정적으로 구동시키는 접근법을 제시하여, 리치에이션 상태가 전극의 초기 반응성/가역성 및 구조 안정성에 결정적임을 밝혔다[13]. Wu 등은 화학적 리치에이션을 통해 LixFeFe(CN)6 (x=0-2) 계열을 제어하고, Li-rich 상태에서의 안정적인 양극 구동 가능성을 보고하였다[21].
정리하면, PB계가 LIB에서 양극으로 작동하기 위해서는 프레임워크 결함/수분의 정밀 제어로 구조적/계면적 불안정을 최소화하고, 리치에이션으로 초기 전하 상태 및 삽입 자리를 사전에 조절하며, 전해질/CEI 환경을 PB계에 유리하도록 맞추는 접근이 필요하다. 또한, 일반적으로 공침법 기반 합성에서는 Li4Fe(CN)6 전구체가 상용적으로 존재하지 않기 때문에, Li2FeFe(CN)6을 합성 단계에서 직접적으로 제조하는 것이 불가능하다는 근본적 제약이 있으며[20], 이로 인해 LIB full-cell 적용을 위해서는 화학적/전기화학적 prelithiation 전략이 중요한 전제 조건이 된다.
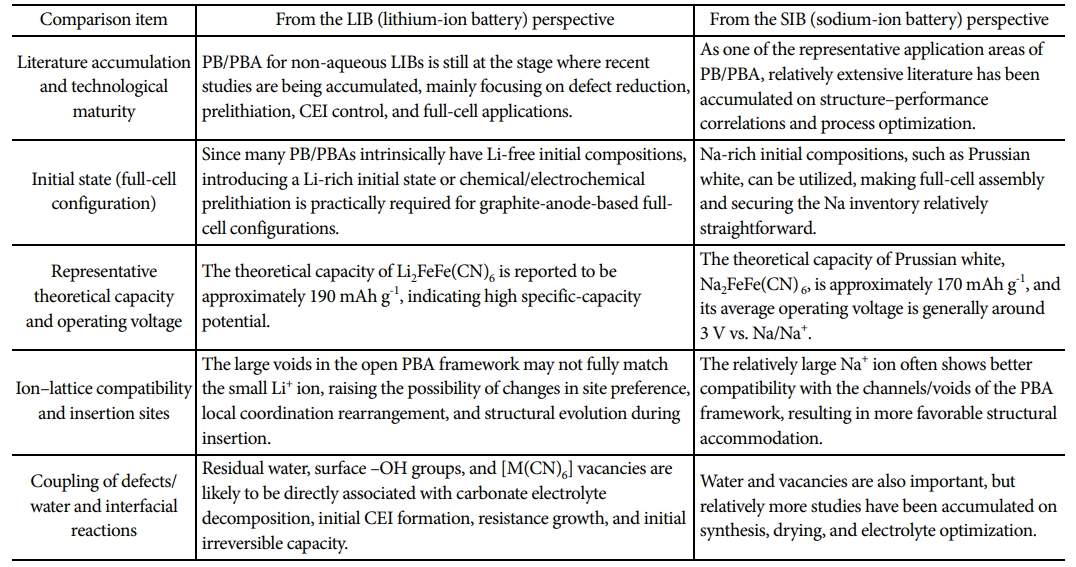
PB/PBA는 개방형 채널 골격으로 다양한 이온 저장이 가능하나, 실제로는 Na-PBA가 SIB에서 가장 활발히 연구되어 왔다. Table 1은 LIB에서 추가로 요구되는 설계 요소를 SIB와 대조해 요약한다.
|
Fig. 2 Structural changes in PB/PBA. (a) Schematic illustration of the lattice structure during stepwise delithiation from Li2FeIIFeII(CN)6 to LiFeIIFeIII(CN)6 and FeIIIFeIII(CN)6. Reprinted from [13] under the CC BY 4.0 license. Spin-state differences of coordinated metals depending on the coordination environment: (b) low-spin FeC6, (c) high-spin FeN6, and (d) high-spin MnN6. Reprinted from [34] under the CC BY 4.0 license |
4.1 전해질/첨가제 기반 CEI제어와 계면 안정화
PB/PBA를 비수계 유기 전해질에서 LIB 양극으로 구동할 때, 계면 반응은 초기 CEI 형성과 그 이후의 저항 성장, 전이금속 용출/오염 누적을 통해 분극과 수명 열화를 유도할 수 있다[22,35,36]. 특히 PB/PBA는 합성 기원 [M(CN)6] 공공과 잔존 수분/–OH가 동반되기 쉬워, 층상 산화물(LCO/NCM)과 달리 전해질 분해의 시작점과 반응 경로, CEI 조성(유/무기 비율 및 폴리머화 경향)이 달라질 가능성이 크다. 따라서 PB/PBA에서는 CEI 형성을 억제하기보다, 저항 성장과 용출을 최소화하는 방향으로 CEI의 형성 경로를 유도하는 것이 현실적인 목표이며, 이를 위해 전해질(염/용매/농도)과 첨가제 설계가 핵심 제어 변수로 작동한다.
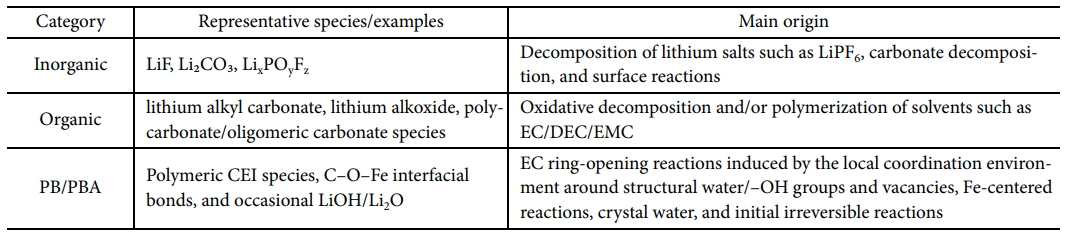
일반적으로 비수계 LIB 양극 표면에서 CEI는 전해질의 전기화학적·화학적 분해와 전극 표면 반응에 의해 형성되는 유·무기 복합 계면층으로 이해된다. 대표적인 구성종으로는 LiF, Li2CO3, LixPOyFz와 같은 무기 성분과, lithium alkyl carbonate, lithium alkoxide, alkyl carbonate, polycarbonate/oligomeric carbonate species와 같은 유기 성분이 보고된다 (Table 2). 이러한 CEI는 전자 차단과 Li+ 전달의 균형을 제공하고, 추가적인 전해질 분해 및 표면 열화를 완화하며, 경우에 따라 전이금속 용출을 억제하는 역할을 할 수 있다. 그러나 CEI가 불균일하거나 과도하게 성장하면 계면 저항 증가와 성능 저하로 이어질 수 있다[37].
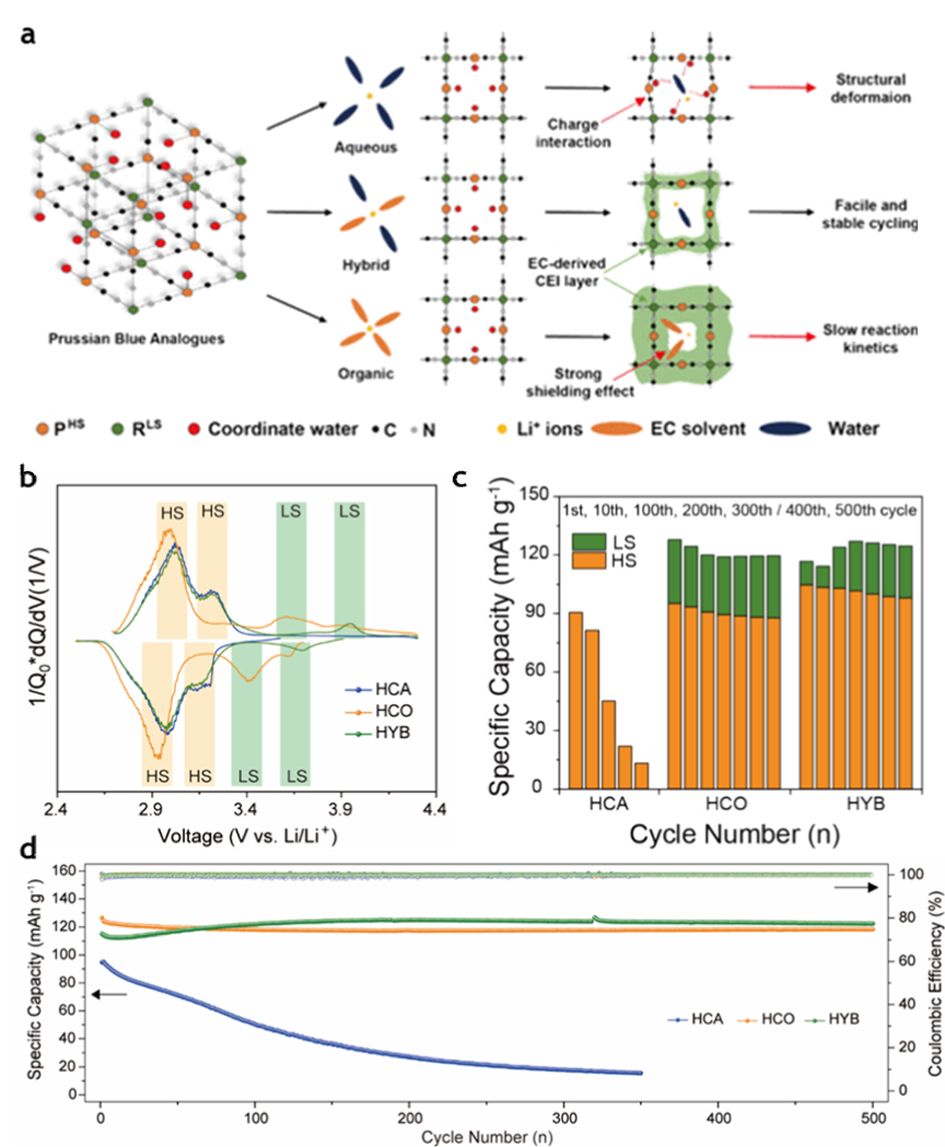
PB/PBA의 경우에는 잔존 구조수와 –OH, 그리고 vacancy 주변의 비포화 금속 배위환경 때문에 CEI 형성 경로가 일반적인 산화물 양극과 다르게 전개될 수 있다. Wi 등은 FeHCFe(iron hexacyanoferrate) 기반 PBA에서 프레임워크 내 구조수/배위수로부터 유래한 OH 관련 라디칼이 EC(ethylene carbonate)의 ring-opening 및 후속 중합을 유도해, 입자 표면에 산소(탄산염/카복실기 등)가 풍부한 고분자성 CEI가 in situ로 형성됨을 제시하였다(Fig. 3)[22]. 전해질 조건(HCA: 21 m LiTFSI in water, HCO: 5.5 m LiTFSI in EC, HYB: HCA+HCO 혼합)에 따라 전압 프로파일과 dQ/dV 피크가 뚜렷이 달라지며, 특히 유기계(HCO)에서는 Fe low-spin (Fe_LS) 레독스 피크(환원/산화: 3.43/3.60 V, 3.70/3.88 V)가 뚜렷하게 나타나는 반면 수계(HCA)에서는 해당 피크가 거의 관찰되지 않는다. 또한 HYB에서는 초기에는 완전한 CEI가 형성되지 않지만 수 회 사이클 이후 견고한 CEI가 안정화되며 Fe_HS와 Fe_LS 사이트가 함께 활성화되고, 이 CEI가 물/하이드로늄 침투 및 charge interaction을 차폐하여 전극 분말화·활성점 소실을 억제함으로써 분극과 구조적 불안정을 완화한다. 그 결과 FeHCFe는 약 120–130 mAh g-1 수준의 용량을 유지하며 500 사이클 이상 안정 구동을 달성하고(HCO에서 500 사이클 용량 유지율 93.6%, HYB에서 500사이클 107%), 수분을 단순 불순물이 아니라 계면 반응 경로(CEI 화학/구조)와 활성 사이트(특히 Fe_LS) 보존을 좌우하는 조절 인자로 다뤄야 함을 시사하였다.
한편 탄산염 전해질 분해(특히 EC 고리열림 포함)는 양극 표면 반응 및 전해질 분해 종(PF5 등)에 의해 촉진될 수 있음이 계산적으로 정리되어 있으며[38], PB/PBA에서도 전해질 분해 반응을 저항 증가가 적고 안정한 CEI로 연결시키는 반응 경로를 확보하는 것이 핵심이다[22].
전해질 설계(염 종류/농도/첨가제)는 용매화(solvation) 구조와 계면 반응을 바꿔 CEI 조성과 용출 거동을 간접적으로 제어할 수 있다. 특히 농축 전해질 또는 용매화 구조를 강하게 재구성하는 조성은 분해 생성물의 조성을 바꾸고 부반응을 완화할 수 있다는 논의가 수계 PBAs에서 체계적으로 정리되어 왔다[12,18]. 다만 비수계 LIB에서는 미량 수분도 초기 CEI 반응을 좌우할 수 있으므로, PB/PBA에서는 염-용매-수분 조건이 CEI 조성/저항 성장/전이금속 용출에 미치는 영향을 전압창/온도/전극 로딩까지 포함해 정량적으로 비교할 필요가 있다.
4.3 전극 설계 전략
4.3.1 미세구조(형상) 기반 전달 저항 저감
앞서 언급한 분극/전하이동 제한을 완화하기 위해서는 전극 수준에서 전자/이온 전달 경로를 동시에 최적화하는 전략이 유효하다. 미세구조(형상) 설계는 전극 수준에서 확산 길이를 줄이고 반응 면적을 늘려 분극을 완화하는 접근이다. 예를 들어, stepwise hollow inverted pyramid 형태의 Na1.13Fe[Fe(CN)6]·3.22H2O(FeHCF-2)는 다공/중공 계층 구조로 전해질-전극 접촉면과 확산 경로를 동시에 최적화하여 분극을 줄이고, 153.7 mAh g-1 (0.1C)에서 92.46 mAh g-1으로의 율속 특성과 1C에서 1000사이클 후에도 용량 유지(≈115 mAh g-1 수준)를 보고하였다[39]. 또한 1C에서 초기 111.88 mAh g-1, 1000 사이클 후 115.04 mAh g-1로 보고되어(사이클 진행 중 활성화 거동 포함) 장기 안정 구동 가능성을 제시하였다. 이러한 형상 설계는 전자전도도 자체를 바꾸기보다는, 전극 내 전달 저항(확산/계면 저항)의 기하학적 성분을 줄이는 방식으로 이해하는 것이 타당하다.
4.3.2 복합재 기반 전도 네트워크 및 계면 안정화
한편 PB/PBA의 낮은 고유 전자전도도는 비수계 LIB에서 전하이동 분극을 유발하는 핵심 요인 중 하나이므로, 복합재 기반 전극 설계는 이를 보완하기 위한 가장 직접적인 전략으로 이해할 수 있다. 복합화는 크게 (i) MXene과 같은 2차원 전도성 소재와의 하이브리드화를 통해 전자 전달과 계면 안정화를 동시에 도모하는 방법, (ii) CNT, graphene, rGO 등 탄소 나노소재를 이용해 입자 간 percolation network를 형성하는 방법, (iii) PANI, PPy, PEDOT계 전도성 고분자를 이용해 표면 코팅 또는 바인더 하이브리드화를 구현하는 방법으로 구분될 수 있다.
예를 들어, 2D 전도성 소재인 MXene(Ti3C2Tx)을 이용한 복합화는 PB/PBA 입자 주위에 연속적인 전도 네트워크를 제공해 전극 내 분극을 줄이는 데 유효하다[23]. FeFe(CN)6-Ti3C2Tx 하이브리드에서는 EIS로 확인한 전하이동저항이 468 Ω에서 105 Ω로 감소했고, Li+ 확산계수도 3.85 × 10-14 cm2 s-1 (Fe–PBA)에서 1.596 × 10-13 cm2 s-1 (Fe–PBA–CT2)로 증가하였다. 이에 따라 0.1C에서 145.9 mAh g-1의 용량을 보였으며, 1C에서 900 사이클 동안 용량 감소가 거의 없는 안정 구동을 보고하였다. 이러한 결과는 MXene 복합화가 전도도 향상에 그치지 않고, 장기 사이클에서의 저항 성장 완화(계면 반응의 누적 억제 포함)로도 연결될 수 있음을 시사한다.
전도성 고분자 복합화 역시 PB/PBA의 복합재료화 관점에서 중요한 전략이다. LIB 양극 사례로, HClO4 도핑 polyaniline(PANI)을 FeFe(CN)6와 in-situ 산화중합으로 결합한 PANI–FeFe(CN)6 복합체는 FeFe(CN)6가 PANI 매트릭스 내에 균일하게 분산된 하이브리드 구조를 형성하였고, 그 결과 bare FeFe(CN)6 대비 향상된 specific capacity, cycling stability, 및 rate capability를 나타냈다. 특히 PANI–FeFe(CN)6 (80%)는 100 사이클 후에도 95.7 mAh g-1의 방전용량을 유지하였고, 20, 50, 100, 200, 500 mA g-1에서 각각 95.9, 98.8, 91.4, 83.6, 72 mAh g-1를 나타내었다. 또한 CV에서는 순수 FeFe(CN)6보다 작은 polarization을 보였고, EIS 분석에서도 charge-transfer resistance가 FeFe(CN)6의 827.3 Ω에서 PANI–FeFe(CN)6(80%)의 198.6 Ω으로 감소하여, 전도성 고분자 복합화가 PB/PBA의 낮은 전자전도도를 보완하면서 전극–전해질 계면에서의 charge transport를 개선할 수 있음을 보여주었다[40]. 저자들은 이러한 향상을 PANI와 FeFe(CN)6 사이의 상호작용과 향상된 전자전도성에 기인한 것으로 해석하였다.
탄소계 복합화는 전자전도 경로 확보와 표면 반응 완화 측면에서 여전히 중요한 설계 방향이다. PB/PBA 입자 표면 또는 다공성 구조에 graphene, rGO, CNT 등을 결합하면 전자전도 경로가 확보되고, 입자 성장 억제와 반응 면적 증가를 통해 고율 특성 향상도 기대할 수 있다[41–44]. 또한 PVP와 같은 고분자를 브리지로 사용해 PB–탄소 간 결합을 안정화하면 보다 균일한 분산 및 코팅이 가능해지고, 이에 따라 장수명 및 고율 특성이 함께 개선되는 사례가 제시되어 왔다. 다만 비수계 LIB 양극 관점에서는 MXene이나 전도성 고분자 복합화에 비해 CNT/graphene/rGO 기반 전도 네트워크를 체계적으로 비교한 직접 문헌은 아직 제한적이므로, 향후에는 low-defect 또는 lithiated PB/PBA를 기반으로 한 저탄소 함량 복합화와 full-cell 수준 검증이 필요하다.
또한 PVP 등 고분자를 브리지로 사용해 PB–탄소 간 결합을 안정화하면 균일한 분산과 코팅이 가능해지고, 장수명 및 고율 성능이 개선되는 사례가 반복적으로 제시되었다[44]. 전도성 고분자(PANI/PPy 등) 코팅은 전자전도도 향상과 표면 보호를 동시에 노릴 수 있으며, 코팅의 연속성/두께 및 기계적 무결성이 CEI 안정성과 수명에 큰 영향을 준다[16,45]. 또한 core–shell, heterointerface, 다공성 템플릿 기반 구조 등 이종계면 설계는 이온/전자 전달 경로를 분리 또는 병렬화하여 분극을 줄이고 부반응을 억제하는 방법으로 보고되어 왔다[10,45–47].
종합하면, PB/PBA 복합재 설계는 단순한 전도도 향상 전략을 넘어, 전자 전달, 계면 보호, 구조 안정화를 동시에 달성하기 위한 통합적 접근으로 이해하는 것이 타당하다. 특히 비수계 LIB에서는 결함/수분과 CEI 형성이 밀접하게 결합되어 있으므로, 향후 복합화 연구는 복합재 함량, 전극 밀도, 면적용량, full-cell 재현성과 함께 계면 저항 성장까지 함께 제시하는 방향으로 발전할 필요가 있다.
4.4 소재 설계 및 초기 상태
장기 열화 관점에서 전이금속 용출은 계면 조성을 지속적으로 바꾸고, 재침전/오염이 누적되면 저항 증가 및 용량 저하를 유발할 수 있는 대표 메커니즘이다[19]. 따라서 열화가 진행된 뒤를 억제하는 접근뿐 아니라, 계면 반응이 시작되는 출발 조건 자체를 안정화하는 소재 설계가 중요하다. PB/PBA는 수용액 공침, 킬레이트/첨가제 보조, 용매열/이온열 합성 등으로 발전해 왔으며, 이 과정에서 공공과 수화도를 낮추거나 특정 결함 형태를 제어하는 전략이 제시되어 왔다[7,10]. 일반적으로 공공/수화가 줄어들면 구조 안정성은 향상되지만, 입자 성장 및 확산 경로 변화가 동반되어 고율 특성이 불리해질 수 있는 trade-off가 보고되어 왔다[48]. 따라서 LIB 양극 관점에서는 비수계에서 불리한 수분/불안정 결함을 최소화하되, Li+ 전달에 유리한 미세구조·확산 경로를 유지하는 균형 설계가 필요하다.
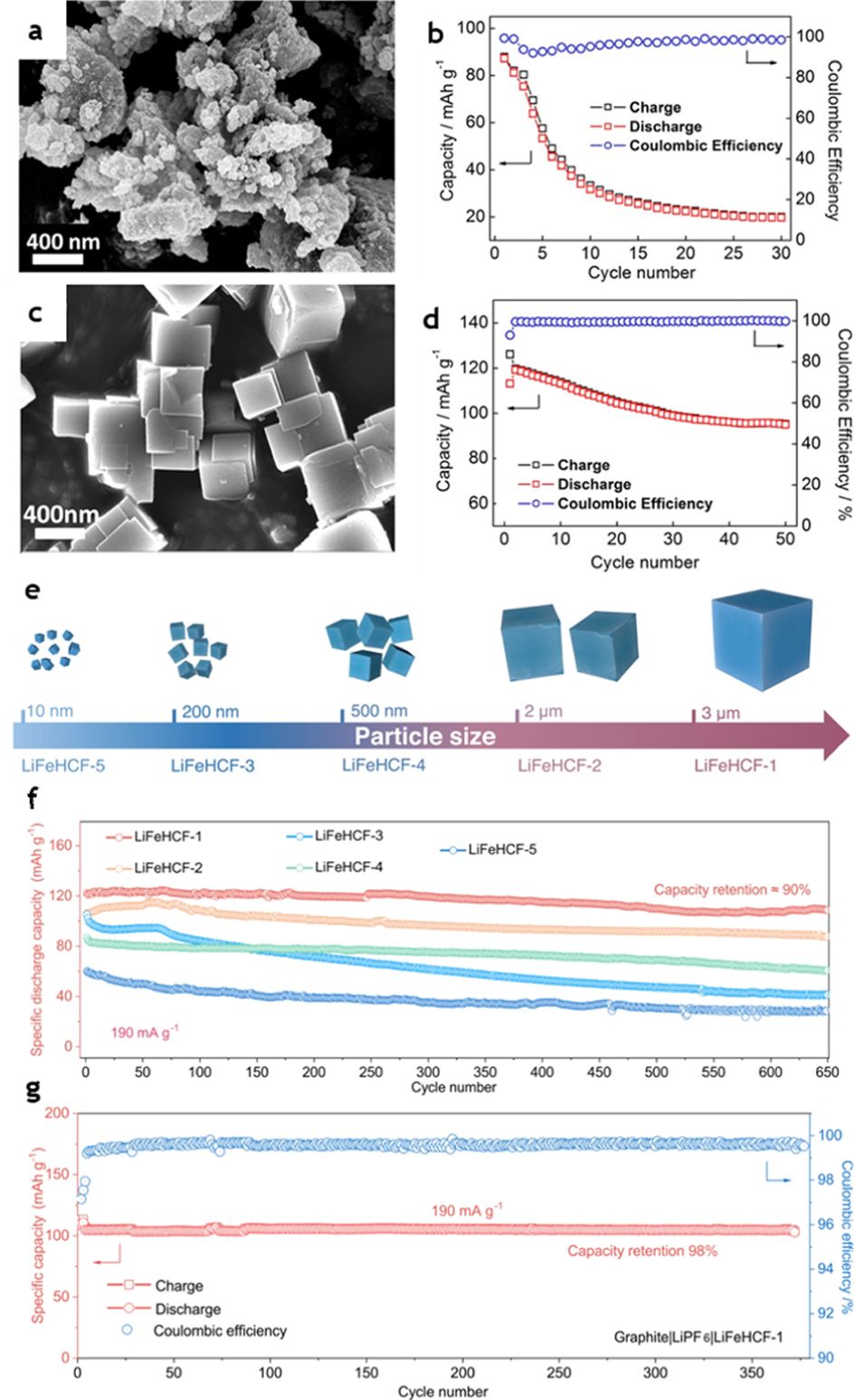
저결함 프레임워크의 중요성은 Wu 등의 결과가 대표적이다. 이들은 PB/PBA에서 흔히 동반되는 [Fe(CN)6] 공공(vacancy)과 그에 연계된 구조수/배위수가 활성 사이트를 감소시키고, 삽입·탈리 과정에서 국소 구조 왜곡과 계면 부반응을 키워 가역 용량과 수명 열화로 이어질 수 있다는 점에 주목하였다[22]. 실제로 저결함 FeFe(CN)₆는 조성 자체가 Fe[Fe(CN)6]0.94□0.06·1.6H2O(공공 6%, 낮은 수분 함량)에 근접하도록 제어되었고[20], 2.0-4.3 V(vs Li/Li+)에서 160 mAh g-¹, 24C에서 102 mAh g-¹, 3C에서 300 사이클 후 약 90% 용량 유지를 보고하였다(Fig. 4a-b). 반대로 공공이 큰 Fe[Fe(CN)6]0.71□0.29·4.6H2O(29% vacancy)는 초기 용량이 87 mAh g-¹에 그쳤고, 10사이클에서 32 mAh g-¹까지 급격히 저하되었다(Fig. 4c-d). 또한 중간 결함 Fe[Fe(CN)6]0.87□0.13· 3.1H2O(13% vacancy)도 초기 120 mAh g-1에서 50사이클 후 95 mAh g-1로 감소(약 79%)하여, 결함/수분 저감이 수명 안정성의 핵심 설계변수임을 보여준다. 이처럼 결함·수분 저감은 단순 구조 안정성을 넘어 활성 레독스 사이트 확보 (특히 저스핀/고스핀 Fe 레독스 활용) 및 계면 부반응 억제와 연결되어, 비수계에서의 고율/장수명 구동으로 직결될 수 있다.
PB/PBA를 비수계 LIB 양극으로 확장할 때의 병목은 Li-free 출발 상태에서의 초기 불가역 반응과 결함·수분에 따른 Li 이동/구조 불안정인데, Zhang 등은 이를 초기 상태 설계(리치에이션) 문제로 보고 lithiated PBA(Li2-xFeFe(CN)6· nH2O)로 출발 조성을 맞추는 전략을 제시했다[13]. 또한 샘플 간 다른 입자 크기/형상을 제시하며 형태학적 출발 조건이 분극/확산(kinetics)과 계면 안정성에 함께 영향을 준다는 점을 전제로 하고(Fig. 4e), 중성자 회절/operando XRD/BVEL 계산로 Li 점유(x)와 수분(n)이 Li 확산 네트워크 및 구조 안정성을 어떻게 바꾸는지 보고하였다. 이러한 설계 관점에서 저자들은 마이크론 크기의 단결정 형태학과 낮은 결함/수분(특히 zeolitic water) 조건을 갖는 LiFeHCF-1을 대표 샘플로 선택했으며, Li 금속 하프셀에서 초기 방전용량 142 mAh g-1@19 mA g-1, 그리고 1.9 A g-1에서 1000 사이클 후 80.7% 유지를 보고하였다[13]. 또한 흑연 음극으로 확장한 풀셀에서도 190 mA g-1에서 약 105 mAh g-1 수준의 안정 용량과 370 사이클에서 98% 유지를 보이며(Fig. 4g), 리치에이션 상태의 제어가 PB 기반 리튬이온 배터리의 실용 구동의 관문임을 강조하였다.
Wu 등은 Li-rich PB 구현을 위해 포텐셜 매칭(potential matching) 원리에 기반한 화학적 리치에이션 방법론을 제안하였다[21]. 즉, FeFe(CN)6의 과환원(Fe2+→Fe0) 및 프레임워크 붕괴가 시작되는 전위(약 0.94 V vs. Li/Li+)보다 높은 산화환원 전위를 갖는 리치에이션 시약을 선택해야 하며, 이에 따라 perylene-Li(~1.28 V vs. Li/Li+)를 선별해 과리치에이션에 의한 구조 붕괴를 피하면서 FeFe(CN)6를 Li2FeFe(CN)6 수준까지 제어 가능하게 리치에이션하였다[21]. 완전 리치에이션된 Li2FeFe(CN)6는 2-4.2 V(vs. Li/Li+) 범위에서 153.3/155.9 mAh g-1(초기 charge/discharge, 거의 100% 초기 CE)를 보였고, 10C에서 1000 사이클 동안 초기 용량의 약 60% 유지를 보고하였다. 이 방법론은 리치에이션 깊이(x=0-2)를 단계적으로 조절할 수 있어, 결함/수분/상(phase)과 초기 상태가 CEI 형성 및 분극 성장에 미치는 영향을 체계적으로 비교할 수 있는 플랫폼으로도 의미가 있다.
이러한 결과는 PB계의 LIB 양극화를 가능성에서 재현 가능한 공정으로 이동시키는 핵심 근거가 된다. 또한, 결함 치유(defect healing) 및 결정상 제어(monoclinic/rhombohedral 등)는 삽입 이온의 정렬과 상전이 경로를 바꿔 전압 프로파일과 구조 안정성에 영향을 줄 수 있으며, 반복 삽입에 따른 구조 변형과 응력 누적을 완화하는 방향으로 활용될 수 있다[10,49-51].
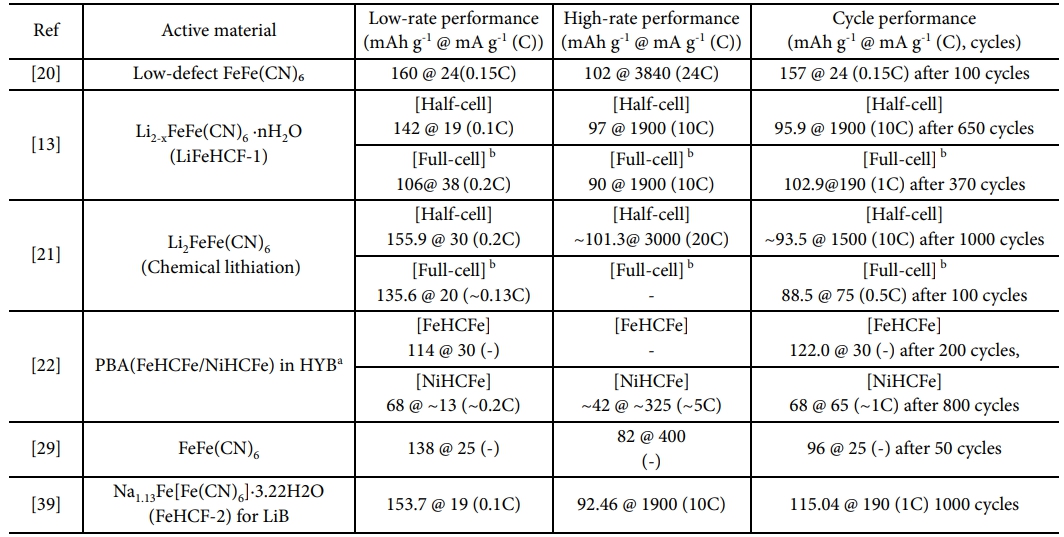
다만 복합화 성능은 전극 로딩·면적용량·공극률·전해질 조건에 민감하므로, 실용성 논의에서는 면적용량/로딩, 전극 밀도·공극률, 풀셀 조건(N/P), 온도 의존성을 함께 제시하는 것이 필요하다. PB계 양극의 LIB 적용에서 문헌 간 전극 조건 (로딩, 전해질, 전압창, 활성화 과정)이 상이하므로 절대 비교에는 한계가 있으며, 향후 후속 연구들의 축척이 필요하다. Table 3은 비수계 LIB에서 PB/PBA의 대표 보고를 성능 축(저율–고율–수명)으로 나란히 정리해, 어떤 설계가 어떤 지표를 개선했는지 한눈에 비교하도록 구성하였다.
|
Fig. 3 Lithium ion insertion reactions and CEI formation in the PBA (FeHCFe) cathode as a function of electrolyte composition (aqueous/organic/hybrid), and the resulting changes in electrochemical performance. (a) Schematic illustration of CEI formation and structural stabilization in different electrolytes. (b) Comparison of dQ/dV curves under HCA, HCO, and HYB conditions. (c) Changes in the capacity contributions of HS and LS sites during cycling. (d) Long-term cycling performance and coulombic efficiency. Reprinted from [22] under the CC BY 4.0 license |
|
Fig. 4 Morphology–performance correlations of PB/PBA cathodes through defect (vacancy/structural water) and particle-size control. (a,b) SEM images of a high-defect FeFe(CN)6 sample and its initial cycling behavior (capacity/coulombic efficiency). (c,d) SEM images of low-defect FeFe(CN)6 nanocubes and their improved cycling stability/coulombic efficiency. Reprinted with permission from [20]. (e) Schematic illustration of particle-size design for lithiated PBA (LiFeHCF). (f) Comparison of the long-term cycling performance of LiFeHCF-1 to LiFeHCF-5. (g) Longterm cycling performance and coulombic efficiency of the full cell. Reprinted from [13] under the CC BY 4.0 license |
|
Table 3 Electrochemical performance of Prussian blue/PBA cathodes in non-aqueous LIBs |
a Hybrid Electrolyte (LiTFSI in water and EC) b Graphite Anode |
상용 LIB 양극의 관점에서 보면, NCM 계열과 LFP는 각각 고에너지 밀도와 장수명/저가/안전성의 대표 기준점으로 기능한다. IEA는 2024년 기준 LFP 배터리 팩이 NMC 팩보다 kWh당 가격이 거의 30% 낮은 반면, 에너지 밀도는 질량 기준 약 20%, 부피 기준 약 1/3 낮다고 정리하였다. 반면, NMC 배터리는 장거리 주행이나 저온 구동과 같이 높은 에너지 밀도가 필요한 응용에서 여전히 우위를 가지는 것으로 평가된다. 이러한 특성은 Ni-rich NCM811 양극 문헌에서도 확인되며, 0.25 wt% SiO2-coated LiNi0.8Co0.1Mn0.1O2는 초기 방전용량 200.7 mAh g-¹와 0.5 C에서 100사이클 후 87.3%의 용량 유지율을 나타내어, 높은 실용 비용량과 준수한 사이클 안정성을 동시에 보여주었다[52].
반면 LFP의 강점은 단순한 소재 단위 비용량보다는, 실제 시스템 수준에서 입증된 긴 수명과 높은 안전성에 있다. 예를 들어 BYD는 자사 Blade Battery(LFP)에 대해 5,000회 이상의 충/방전 사이클, 8년 또는 250,000 km의 보증(SOH 70% 이상), 그리고 nail penetration test 통과를 제시하고 있으며, 회사 비교표에서는 전통적인 NCM 배터리를 약 1,000-2,000 cycles 수준으로 제시하고 있다. 물론 이러한 수치는 기업이 제시한 시스템 수준 지표이므로 전극 단위 논문 성능과 직접 비교되지는 않지만, 적어도 LFP가 현재 산업계에서 고에너지 밀도보다는 장수명/안전성/저원가의 축으로 확고한 상용적 위치를 확보했음을 보여준다.
이러한 비교 축에서 PB/PBA는 단기적으로 NCM을 직접 대체하는 고에너지 양극이라기보다는, LFP와 유사한 저원가/안전성 지향 양극 플랫폼으로 해석하는 것이 보다 타당하다. 앞서 언급된 Zhang 등의 연구에서 lithiated PBA인 Li2-xFeFe(CN)6·nH2O(LiFeHCF-1)는 Li metal half-cell에서 초기 방전용량 142 mAh g-1@19 mA g-1를 나타내었고, 1.9 A g-1의 고율 조건에서도 1000사이클 후 80.7%의 용량 유지율을 보였다[13]. 더 나아가 graphite 기반 full-cell에서도 190 mA g-1에서 약 105 mAh g-1의 안정 용량과 370사이클 후 98%의 용량 유지율이 보고되어, PB/PBA가 half-cell 수준을 넘어 full-cell 관점에서도 유의미한 안정성을 확보할 수 있음을 보여주었다. 이러한 수치는 NCM811의 높은 비용량에는 아직 미치지 못하지만, LFP에 근접한 gravimetric capacity와 장수명 안정성의 가능성을 시사하며, 특히 graphite full-cell에서 100 mAh g-1 내외의 안정 용량이 수백 사이클 이상 유지된다는 점은 저가형 LIB 양극 후보로서 충분한 의미를 가진다.
안전성 측면에서도 세 양극재의 상대적 위치는 구분된다. 100% SOC 조건에서 수행한 DSC 비교 연구에서는 NMC811이 약 212oC와 259oC 부근에서 뚜렷한 발열 피크를 보인 반면, LFP에서는 유의한 발열 피크가 관찰되지 않으며 높은 열적 안정성을 보였다[53]. PB/PBA의 경우 앞서 2절에서 언급되었던 대로, 수분 환경에서 상온 합성이 이루어져 수분에 의한 열적 안정성 조사가 아직 미흡한 상태이며, 셀/모듈/팩 수준의 안전성 데이터 또한 LFP나 NCM만큼 축적되어 있지 않다. 따라서 현 단계에서 PB/PBA의 산업적 위치는 NCM형 고에너지 장거리 EV용 양극보다는, 비용과 자원성, 그리고 안전성이 중요한 중/저에너지 밀도 응용을 지향하는 차세대 저가형 LIB 양극 후보로 정리하는 것이 적절하다. 향후에는 고밀도 전극 구현, 낮은 탄소 함량의 복합화, graphite 기반 full-cell의 장기 재현성, 그리고 표준화된 열적 안정성 평가가 함께 축적되어야 PB/PBA의 실질적인 상용 경쟁력을 보다 명확히 판단할 수 있을 것이다.
PB/PBA는 개방형 프레임워크와 비교적 풍부한 원소 기반 조성이라는 장점에도 불구하고, 비수계 LIB 양극에서는 전달 저항(분극)과 계면 불안정(CEI/용출)이 성능과 수명을 동시에 제한해 왔다. 최근 연구는 이 두 축을 분리해서가 아니라 동시에 해결하려는 방향으로 전개되고 있다. 저결함 프레임워크는 높은 가역 용량과 고율·장수명 특성을 함께 달성할 수 있음을 보여주었고[20], 리치에이션은 비수계에서 안정적으로 동작 가능한 초기 상태를 제공함으로써 가역성과 안정성을 개선할 수 있음을 제시했다[13,21]. 또한 CEI 엔지니어링 관점은 전해질 분해를 단순 부반응으로 보기보다, 저항 성장과 용출을 억제하는 계면 반응 경로를 설계하는 문제로 전환시켰고, PB/PBA에서도 실질적인 장기 안정화 사례가 보고되었다[22].
상용 LIB 양극으로의 진입을 위해서는 (i) 공공/수화도의 정량 표준화, (ii) CEI의 특성 분석(이온전도/전자차단/기계적 안정)과 성능의 상관관계 확립, (iii) 고면적용량 조건에서의 전극 설계 최적화(전도 네트워크/공극/집전체), (iv) 풀셀 기반(N/P, 로딩 매칭, 온도 조건) 재현성 검증이 요구된다[13]. 특히 출력과 안정성을 동시에 만족시키려면 PB 자체의 품질, 초기 상태, 계면 반응 등을 한 번에 최적화하는 접근이 필수적이다.
또한 PB계 프레임워크는 최근 LIB 음극에서도 활발히 보고되며, 일부 연구에서는 높은 반응성 및 준수한 속도 특성을 제시하고 있어[54], LIB에서 양극뿐 아니라 음극에서도 유망한 전극 소재군으로 확장될 수 있음을 시사한다. 이는 전극의 극성이 달라도 결함/수분/표면화학이 계면층 형성 및 저항 성장에 영향을 주어 성능을 좌우한다는 점에서, 양극과 음극이 공유하는 공통 과제가 존재함을 보여준다. 따라서 PB/PBA는 적절한 품질/계면 제어가 뒷받침될 경우, 차세대 저원가 전극 소재로서의 실용화 가능성을 충분히 갖는다.
본 연구는 산업통산자원부(MOTIE)와 한국에너지기술평가원(KETEP)의 지원을 받아 수행한 연구 과제입니다. (No.RS-2024-00402410)
- 1. Tarascon, J.M., and Armand, M., “Issues and Challenges Facing Rechargeable Lithium Batteries,” Nature, Vol. 414, 2001, pp. 359–361.
- 2. Whittingham, M.S., “Lithium Batteries and Cathode Materials,” Chemical Reviews, Vol. 104, No. 10, 2004, pp. 4271–4302.
-

- 3. Islam, M.S., and Fisher, C.A.J., “Lithium and Sodium Battery Cathode Materials: Computational Insights into Voltage, Diffusion and Nanostructural Properties,” Chem. Soc. Rev., Vol. 43, No. 1, 2014, pp. 185–204.
-

- 4. Adebanjo, I.T., Eko, J., Agbeyegbe, A.G., Yuk, S.F., Cowart, S.V., Nagelli, E.A., Burpo, F.J., Allen, J.L., Tran, D.T., Bhattarai, N., Shah, K., Hwang, J.-Y., and Sun, H.H., “A Comprehensive Review of Lithium-ion Battery Components Degradation and Operational Considerations: A Safety Perspective,” Energy Advances, Vol. 4, No. 7, 2025, pp. 820–877.
-

- 5. Manthiram, A., “A Reflection on Lithium-ion Battery Cathode Chemistry,” Nature Communications, Vol. 11, No. 1, 2020, pp. 1550.
-

- 6. Whittingham, M.S., “Ultimate Limits to Intercalation Reactions for Lithium Batteries,” Chemical Reviews, Vol. 114, No. 23, 2014, pp. 11414–11443.
-

- 7. Hurlbutt, K., Wheeler, S., Capone, I., and Pasta, M., “Prussian Blue Analogs as Battery Materials,” Joule, Vol. 2, No. 10, 2018, pp. 1950–1960.
-

- 8. Wang, Q., Li, J., Jin, H., Xin, S., and Gao, H., “Prussian‐blue Materials: Revealing New Opportunities for Rechargeable Batteries,” InfoMat, Vol. 4, No. 6, 2022, pp. e12311.
-

- 9. Palaganas, M.S., Garcia, J.S., Sanglay, G.D.D., Sapanta, L.M.E., Limjuco, L.A., and Ocon, J.D., “Can Prussian Blue Analogues be Holy Grail for Advancing Post‐Lithium Batteries?,” Batteries & Supercaps, Vol. 7, No. 10, 2024, pp. e202400280.
-

- 10. Xiao, Y., Xiao, J., Zhao, H., Li, J., Zhang, G., Zhang, D., Guo, X., Gao, H., Wang, Y., Chen, J., Wang, G., and Liu, H., “Prussian Blue Analogues for Sodium‐Ion Battery Cathodes: A Review of Mechanistic Insights, Current Challenges, and Future Pathways,” Small, Vol. 20, No. 35, 2024, pp. 2401957.
-

- 11. Bai, Y., YuChi, K., Liu, X., Tian, S., Yang, S., Qian, X., Ma, B., Fang, M., Liu, Y., Huang, Z., and Min, X., “Progress of Prussian Blue and Its Analogues as Cathode Materials for Potassium Ion Batteries,” European Journal of Inorganic Chemistry, Vol. 26, No. 25, 2023, pp. e202300246.
-

- 12. Xu, C., Yang, Z., Zhang, X., Xia, M., Yan, H., Li, J., Yu, H., Zhang, L., and Shu, J., “Prussian Blue Analogues in Aqueous Batteries and Desalination Batteries,” Nano-Micro Letters, Vol. 13, No. 1, 2021, pp. 166.
-

- 13. Zhang, Z., Avdeev, M., Chen, H., Yin, W., Kan, W.H., and He, G., “Lithiated Prussian Blue Analogues as Positive Electrode Active Materials for Stable Non-aqueous Lithium-ion Batteries,” Nature Communications, Vol. 13, No. 1, 2022, pp. 7790.
-

- 14. Xiao, P., Song, J., Wang, L., Goodenough, J.B., and Henkelman, G., “Theoretical Study of the Structural Evolution of a Na2 FeMn(CN)6 Cathode upon Na Intercalation,” Chemistry of Materials, Vol. 27, No. 10, 2015, pp. 3763–3768.
-

- 15. Hegner, F.S., Galán-Mascarós, J.R., and López, N., “A Database of the Structural and Electronic Properties of Prussian Blue, Prussian White, and Berlin Green Compounds through Density Functional Theory,” Inorganic Chemistry, Vol. 55, No. 24, 2016, pp. 12851–12862.
-

- 16. Hurlbutt, K., Giustino, F., Pasta, M., and Volonakis, G., “Electronic Structure and Electron-Transport Properties of Three Metal Hexacyanoferrates,” Chemistry of Materials, Vol. 33, No. 17, 2021, pp. 7067–7074.
-

- 17. Gebert, F., Cortie, D.L., Bouwer, J.C., Wang, W., Yan, Z., Dou, S., and Chou, S., “Epitaxial Nickel Ferrocyanide Stabilizes Jahn–Teller Distortions of Manganese Ferrocyanide for Sodium‐Ion Batteries,” Angewandte Chemie International Edition, Vol. 60, No. 34, 2021, pp. 18519–18526.
-

- 18. Chen, L., Sun, W., Xu, K., Dong, Q., Zheng, L., Wang, J., Lu, D., Shen, Y., Zhang, J., Fu, F., Kong, H., Qin, J., and Chen, H., “How Prussian Blue Analogues Can Be Stable in Concentrated Aqueous Electrolytes,” ACS Energy Letters, Vol. 7, No. 5, 2022, pp. 1672–1678.
-

- 19. Li, W., “Review—An Unpredictable Hazard in Lithium-ion Batteries from Transition Metal Ions: Dissolution from Cathodes, Deposition on Anodes and Elimination Strategies,” Journal of The Electrochemical Society, Vol. 167, No. 9, 2020, pp. 090514.
-

- 20. Wu, X., Shao, M., Wu, C., Qian, J., Cao, Y., Ai, X., and Yang, H., “Low Defect FeFe(CN)6 Framework as Stable Host Material for High Performance Li-Ion Batteries,” ACS Applied Materials & Interfaces, Vol. 8, No. 36, 2016, pp. 23706–23712.
-

- 21. Wu, C., Hu, J., Chen, H., Zhang, C., Xu, M., Zhuang, L., Ai, X., and Qian, J., “Chemical Lithiation Methodology Enabled Prussian Blue as a Li-rich Cathode Material for Secondary Li-ion Batteries,” Energy Storage Materials, Vol. 60, 2023, pp. 102803.
-

- 22. Wi, T.-U., Park, C., Ko, S., Kim, T., Choi, A., Muralidharan, V., Choi, M., and Lee, H.-W., “Cathode Electrolyte Interphase Engineering for Prussian Blue Analogues in Lithium-Ion Batteries,” Nano Letters, Vol. 24, No. 25, 2024, pp. 7783–7791.
-

- 23. Zhang, N., Qiu, L., Liu, X., Wang, P.-F., Zhu, Y.-R., and Yi, T.-F., “Prussian Blue Analogue Vigorously Coupled to Ti3C2T MXene Nanosheet Toward High-performance Li-ion Batteries with Stable Cycling Stability,” Ceramics International, Vol. 49, No. 11, 2023, pp. 17668–17679.
-

- 24. Yabuuchi, N., Kubota, K., Dahbi, M., and Komaba, S., “Research Development on Sodium-Ion Batteries,” Chemical Reviews, Vol. 114, No. 23, 2014, pp. 11636–11682.
-

- 25. Delmas, C., “Sodium and Sodium‐Ion Batteries: 50 Years of Research,” Advanced Energy Materials, Vol. 8, No. 17, 2018, pp. 1703137.
-

- 26. Wu, X., Zhang, Q., Zhou, X., Zhao, Y., Hoa, N.D., Zeng, R., Yuan, Z., and Wu, X.-L., “Key Issues, Material Design and Application of Prussian Blue and Its Analogues Composites in Metal-ion Based Energy Storage Devices,” Chemical Engineering Journal, Vol. 525, 2025, pp. 170281.
-

- 27. Lee, H.-W., Pasta, M., Wang, R.Y., Ruffo, R., and Cui, Y., “Effect of the Alkali Insertion Ion on the Electrochemical Properties of Nickel Hexacyanoferrate Electrodes,” Faraday Discuss., Vol. 176, 2014, pp. 69–81.
-

- 28. Ling, C., Chen, J., and Mizuno, F., “First-Principles Study of Alkali and Alkaline Earth Ion Intercalation in Iron Hexacyanoferrate: The Important Role of Ionic Radius,” The Journal of Physical Chemistry C, Vol. 117, No. 41, 2013, pp. 21158–21165.
-

- 29. Shen, L., Wang, Z., and Chen, L., “Prussian Blues as a Cathode Material for Lithium Ion Batteries,” Chemistry – A European Journal, Vol. 20, No. 39, 2014, pp. 12559–12562.
-

- 30. Imanishi, N., Morikawa, T., Kondo, J., Takeda, Y., Yamamoto, O., Kinugasa, N., and Yamagishi, T., “Lithium Intercalation Behavior into Iron Cyanide Complex as Positive Electrode of Lithium Secondary Battery,” Journal of Power Sources, Vol. 79, Issue 2, 1999, pp. 215-219.
-

- 31. Asakura, D., Okubo, M., Mizuno, Y., Kudo, T., Zhou, H., Ikedo, K., Mizokawa, T., Okazawa, A., and Kojima, N., “Fabrication of a Cyanide-Bridged Coordination Polymer Electrode for Enhanced Electrochemical Ion Storage Ability,” The Journal of Physical Chemistry C, Vol. 116, No. 15, 2012, pp. 8364–8369.
-

- 32. Zhang, H., Li, J., Liu, J., Gao, Y., Fan, Y., Liu, X., Guo, C., Liu, H., Chen, X., Wu, X., Liu, Y., Gu, Q., Li, L., Wang, J., and Chou, S.-L., “Understanding Capacity Fading from Structural Degradation in Prussian Blue Analogues for Wide-temperature Sodium-ion Cylindrical Battery,” Nature Communications, Vol. 16, No. 1, 2025, pp. 2520.
-

- 33. Maddar, F.M., Walker, D., Chamberlain, T.W., Compton, J., Menon, A.S., Copley, M., and Hasa, I., “Understanding Dehydration of Prussian White: from Material to Aqueous Processed Composite Electrodes for Sodium-ion Battery Application,” Journal of Materials Chemistry A, Vol. 11, No. 29, 2023, pp. 15778–15791.
-

- 34. Xu, Y., Titirici, M., Chen, J., Cora, F., Cullen, P.L., Edge, J.S., Fan, K., Fan, L., Feng, J., Hosaka, T., Hu, J., Huang, W., Hyde, T.I., Imtiaz, S., Kang, F., Kennedy, T., Kim, E.J., Komaba, S., Lander, L., Le Pham, P.N., Liu, P., Lu, B., Meng, F., Mitlin, D., Monconduit, L., Palgrave, R.G., Qin, L., Ryan, K.M., Sankar, G., Scanlon, D.O., Shi, T., Stievano, L., Tinker, H.R., Wang, C., Wang, H., Wang, H., Wu, Y., Zhai, D., Zhang, Q., Zhou, M., and Zou, J., “2023 Roadmap for Potassium-ion Batteries,” Journal of Physics: Energy, Vol. 5, No. 2, 2023, pp. 021502.
-

- 35. Asakura, D., Li, C.H., Mizuno, Y., Okubo, M., Zhou, H., and Talham, D.R., “Bimetallic Cyanide-Bridged Coordination Polymers as Lithium Ion Cathode Materials: Core@Shell Nanoparticles with Enhanced Cyclability,” Journal of the American Chemical Society, Vol. 135, No. 7, 2013, pp. 2793–2799.
-

- 36. Sungjemmenla, S.K., V., Soni, C.B., Kumar, V., and Seh, Z.W., “Understanding the Cathode–Electrolyte Interphase in Lithium‐Ion Batteries,” Energy Technology, Vol. 10, No. 9, 2022, pp. 2200421.
-

- 37. Xu, J., “Critical Review on Cathode–electrolyte Interphase Toward High-Voltage Cathodes for Li-Ion Batteries,” Nano-Micro Letters, Vol. 14, No. 1, 2022, pp. 166.
-

- 38. Tebbe, J.L., Fuerst, T.F., and Musgrave, C.B., “Degradation of Ethylene Carbonate Electrolytes of Lithium Ion Batteries via Ring Opening Activated by LiCoO2 Cathode Surfaces and Electrolyte Species,” ACS Applied Materials & Interfaces, Vol. 8, No. 40, 2016, pp. 26664–26674.
-

- 39. Chang, H., Qiu, L.-Y., Chen, Y.-H., Wang, P.-F., Zhu, Y.-R., and Yi, T.-F., “Rational Construction of Prussian Blue Analogue with Inverted Pyramid Morphology as Ultrastable Cathode Material for Lithium-ion Battery,” Composites Part B: Engineering, Vol. 250, 2023, pp. 110434.
-

- 40. Xu, L., Sun, Y., Han, B., and Su, C., “Preparation of Polyaniline/FeFe(CN)6 Composite and its Electrochemical Performance as Cathode Material of Lithium Ion Battery,” Nano, Vol. 15, No. 08, 2020, pp. 2050107.
-

- 41. Wang, H., Wang, L., Chen, S., Li, G., Quan, J., Xu, E., Song, L., and Jiang, Y., “Crystallographic-plane Tuned Prussian-blue Wrapped with RGO: a High-capacity, Long-life Cathode for Sodium-ion Batteries,” Journal of Materials Chemistry A, Vol. 5, No. 7, 2017, pp. 3569–3577.
-

- 42. Luo, J., Sun, S., Peng, J., Liu, B., Huang, Y., Wang, K., Zhang, Q., Li, Y., Jin, Y., Liu, Y., Qiu, Y., Li, Q., Han, J., and Huang, Y., “Graphene-Roll-Wrapped Prussian Blue Nanospheres as a High-Performance Binder-Free Cathode for Sodium-Ion Batteries,” ACS Applied Materials & Interfaces, Vol. 9, No. 30, 2017, pp. 25317–25322.
-

- 43. Wan, P., Xie, H., Zhang, N., Zhu, S., Wang, C., Yu, Z., Chu, W., Song, L., and Wei, S., “Stepwise Hollow Prussian Blue Nanoframes/Carbon Nanotubes Composite Film as Ultrahigh Rate Sodium Ion Cathode,” Advanced Functional Materials, Vol. 30, No. 38, 2020, pp. 2002624.
-

- 44. Wei, Y., Wang, H., Wang, J., Gao, C., Zhang, H., Yuan, F., Dong, J., Zhai, D., and Kang, F., “Polyvinylpyrrolidone-Bridged Prussian Blue/rGO Composite as a High-Performance Cathode for K-Ion Batteries,” ACS Applied Materials & Interfaces, Vol. 13, No. 45, 2021, pp. 54079–54087.
-

- 45. Pan, Z., He, Z., Hou, J., and Kong, L., “Designing CoHCF@FeHCF Core–Shell Structures to Enhance the Rate Performance and Cycling Stability of Sodium‐Ion Batteries,” Small, Vol. 19, No. 45, 2023, pp. 2302788.
-

- 46. Chen, Y., Shi, Y., Chen, J., Liu, H., Pan, X., Jin, Y., and Chen, J., “Microwave-assisted Synthesis of Highly Uniform Prussian Blue@Carbon Cathode Materials for Sodium-ion Batteries,” Journal of Power Sources, Vol. 615, 2024, pp. 235085.
-

- 47. Shi, W., Nie, P., Zhu, G., Hu, B., Yang, J., and Liu, J., “Self-supporting Prussian Blue@CNF Based Battery-capacitor with Superhigh Adsorption Capacity and Selectivity for Potassium Recovery,” Chemical Engineering Journal, Vol. 388, 2020, pp. 124162.
-

- 48. Cai, D., Yang, X., Qu, B., and Wang, T., “Comparison of the Electrochemical Performance of Iron Hexacyanoferrate with High and Low Quality as Cathode Materials for Aqueous Sodium-ion Batteries,” Chemical Communications, Vol. 53, No. 50, 2017, pp. 6780–6783.
-

- 49. Peng, J., Huang, J., Gao, Y., Qiao, Y., Dong, H., Liu, Y., Li, L., Wang, J., Dou, S., and Chou, S., “Defect‐Healing Induced Monoclinic Iron‐Based Prussian Blue Analogs as High‐Performance Cathode Materials for Sodium‐Ion Batteries,” Small, Vol. 19, No. 36, 2023, pp. 2300435.
-

- 50. Wang, L., Song, J., Qiao, R., Wray, L.A., Hossain, M.A., Chuang, Y.-D., Yang, W., Lu, Y., Evans, D., Lee, J.-J., Vail, S., Zhao, X., Nishijima, M., Kakimoto, S., and Goodenough, J.B., “Rhombohedral Prussian White as Cathode for Rechargeable Sodium-Ion Batteries,” Journal of the American Chemical Society, Vol. 137, No. 7, 2015, pp. 2548–2554.
-

- 51. Li, W., Han, C., Cheng, G., Chou, S., Liu, H., and Dou, S., “Chemical Properties, Structural Properties, and Energy Storage Applications of Prussian Blue Analogues,” Small, Vol. 15, No. 32, 2019, pp. 1900470.
-

- 52. Lee, S.-H., Park, G.-J., Sim, S.-J., Jin, B.-S., and Kim, H.-S., “Improved Electrochemical Performances of LiNi0.8Co0.1Mn0.1O2 Cathode via SiO2 Coating,” Journal of Alloys and Compounds, Vol. 791, 2019, pp. 193–199.
-

- 53. El Moutchou, S., Aziam, H., Mansori, M., and Saadoune, I., “Thermal Stability of Lithium-ion batteries: Case Study of NMC811 and LFP Cathode Materials,” Materials Today: Proceedings, Vol. 51, 2022, pp. A1–A7.
-

- 54. Gao, C., Chen, M., Li, J., Lee, S., Sun, T., Wang, X., Zhang, S., Feng, G., Zhai, D., and Kang, F., “A Layered Prussian Blue Analogue as Fast-charging Negative Electrode Material for Lithium-ion Batteries,” Nature Communications, Vol. 16, No. 1, 2025, pp. 10341.
-

 This Article
This Article
-
2026; 39(2): 115-126
Published on Apr 30, 2026
- 10.7234/composres.2026.39.2.115
- Received on Mar 1, 2026
- Revised on Mar 29, 2026
- Accepted on Apr 9, 2026
 Services
Services
- Abstract
1. 서 론
2. 프러시안블루계 소재 개요
3. pb의 리튬이온전지 양극 활용
4. 비수계 전해질에서의 계면/열화 메커니즘과 성능 향상 전략
5. 응용 및 실용화 관점
6. 결론 및 전망
- 후기
- References
- Full Text PDF
Shared
 Correspondence to
Correspondence to
- Il-Kwon Oh
-
* National Creative Research Initiative for Functionally Antagonistic Nano-Engineering, Department of Mechanical Engineering, Korea Advanced Institute of Science and Technology (KAIST), Yuseong-gu, Daejeon, Republic of Korea
- E-mail: ikoh@kaist.ac.kr






 Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.
Copyright ⓒ The Korean Society for Composite Materials. All rights reserved.